Indice del volumen
Volume index
Comité Editorial
Editorial Board
Comité Científico
Scientific Committee
- Factor de necrosis tumoral alfa (FNT)
- Interleucinas: 1, 2, 6, 8.
- Interferón gamma
- Interleucinas: 4, 10
- Antagonistas de receptores de citocinas
- Respuesta inflamatoria local.
- Respuesta inflamatoria sistémica controlada.
- Respuesta inflamatoria sistémica no controlada.
- Disonancia inmunológica.
- Parálisis inmunológicas.
- Aumento del pH gástrico (antiácidos, anti- H2)
- Parálisis intestinal (sedantes, relajantes musculares, decúbito prolongado)
- Administración de antibióticos de amplio espectro.
- Infusión de dietas enterales no estériles directamente en duodeno y yeyuno.
- Factores mecánicos: mucus y empalizada epitelial.
- Factores inmunológicos: disminución de la IgA
- Hipoxia celular: disminución del aporte de O2, aumento de las necesidades titulares y descenso de la capacidad para la extracción de O2.
- Mediadores citotóxicos: radicales libres de O2, factor de necrosis tumoral, factor activador plaquetario.
- Factores nutricionales: Ausencia de estímulo intraluminal, deficiencia del aporte o utilización de glutamina, ácidos grasos de cadena corta.
LA DISFUNCIÓN ORGÁNICA MÚLTIPLE UN SÍNDROME DE RELEVANCIA EN NUESTRA PRÁCTICA. ASPECTOS ETIOLÓGICOS Y FISIOPATOLOGICOS - I.
Maribel Misas Menéndez*, Aleyda Hernández Lara*,
Marcos D. Iraola Ferrer**
*Unidad de Cuidados Intensivos Quirúrgicos, **Unidad de Cuidados Intensivos Polivalentes, Hospital Universitario Dr. Gustavo Aldereguía Lima. Cienfuegos. Cuba
mif @ gal.sld.cu
Rev Electron Biomed / Electron J Biomed 2005;2:23-38
Comentario del revisor, Ramón Díaz-Alersi, MD. Medicina Intensiva. Hospital Puerto Real. Cádiz. Espańa
Comentario del revisor Prof. Martín de Frutos Herranz MD. PhD. Medicina Intensiva. Escuela Universitaria de Enfermería. Universidad de Burgos. Espańa
SUMMARY
MULTIPLE ORGAN DISFUNCTION: A SYNDROME OF OUTSTANDING IMPORTANCE IN OR PRACTICE.
I- ETIOLOGY AND PHYSIOPATHOLOGIC ASPECTS (1ST PART).
The multiple organ dysfunction syndrome is defined as a potentially reversible diminishing in the function of one or more organs which are not capable of keeping the homeostasis without a therapeutic backup. The term dysfunction implies a continuous and dynamic process in the loss of the function of one organ that goes from less to more being the last stage in the end of the function of that organ and that we call it dysfunction. The reversibility of this syndrome and the intensive care unit this paper is just a wider revision of the multiple organ dysfunction syndrome. In this 1st part, we update the concepts and cover the predisposal factors, etiology, physiopathology, epidemiology and the indexes which frequently evaluate the prognosis.
Keywords: Multiple Organ Dysfunction Syndrome, Classification, Etiology, Physiopathology, Intensive Care Unit
RESUMEN
El Síndrome de Disfunción Orgánica Múltiple se define como la disminución potencialmente reversible en la función de uno o más órganos, que son incapaces de mantener la homeostasis sin un sostén terapéutico. El término disfunción implica un proceso continuo y dinámico en la pérdida de la función de un órgano, que va de menos a más, siendo la etapa final en la claudicación de la función de dicho órgano lo que denominamos disfunción. La reversibilidad de este síndrome y la mortalidad que le acompańa hace que se convierta en una entidad prioritaria en las Unidades de Cuidados Intensivos. Este trabajo hace una revisión amplia del Síndrome de Disfunción Orgánica Múltiple, en su primera parte actualiza los conceptos y aborda los factores predisponentes, la etiología, la fisiopatología, la epidemiología y los índices que más frecuentemente evalúan el pronóstico.
Palabras Clave: Síndrome de Disfunción Orgánica Múltiple, Clasificación, Etiología, Fisiopatología, Unidad de Cuidados Intensivos
INTRODUCCION
Las grandes guerras del siglo pasado marcaron hitos en la historia de la Medicina pues la elevada mortalidad, como complicación del choque y el traumatismo, suscitó la búsqueda de soluciones urgentes permitiendo el nacimiento de diversos procedimientos terapéuticos. Lo cual confirma la sentencia de Renán quien dijera: "Los golpes de la adversidad son amargos pero nunca estériles"
La insuficiencia funcional de órganos y sistemas específicos se reconoció como una complicación devastadora en la evolución de estos heridos de guerra. Antes de la primera guerra mundial se identificó la insuficiencia cardiovascular; en la guerra de Corea, la renal y en la de Vietnam, la pulmonar. Tales realidades favorecieron la aparición de la reanimación con líquidos y reposición de sangre como solución ante el número de victimas cobradas por el shock hipovolémico. En la guerra de Corea, la resucitación inicial en los hospitales del frente de batalla llegó a un nivel óptimo, y la insuficiencia renal aguda se comenzó a tratar efectivamente con técnicas de diálisis. Sin embargo, este tratamiento agresivo del shock dio lugar en la guerra de Vietnam, a la aparición de una nueva entidad en los sobrevivientes, el Síndrome de Dificultad Respiratoria del Adulto o edema agudo pulmonar no cardiogénico que revolucionó la ventilación artificial mecánica.1-3
En el ańo 1973 Nicolás Tilney4 describe por primera vez un síndrome clínico caracterizado por la falla progresiva y secuencial de múltiples órganos que se producía en el período post operatorio de pacientes con reparación de aneurismas de la aorta abdominal. La secuencia se originaba generalmente con falla circulatoria, seguida precozmente de falla ventilatoria y más tardíamente por falla hepática, gastrointestinal y metabólica. Posteriormente dos ańos más tarde, Arthur Baue5 al analizar autopsias de pacientes sometidos a períodos de reanimación prolongada en Unidades de Cuidados Intensivos (UCI), estableció la existencia de elementos anatomo-patológicos comunes en aquellos que cursaron con falla de múltiples órganos. Destacando que dichas alteraciones se encontraban relacionadas unas con otras, pero su mecanismo era en ese entonces aún desconocido.
En la década de los 80, algunos autores6-8 precisan el término, profundizan en su fisiopatología y su diagnóstico relacionando su frecuencia en los pacientes críticos. En 1985, Goris9 establece la existencia de cuadros de fallo multiorgánico en enfermos cuya patología inicial era tanto de origen infeccioso (sepsis intrabdominal) como no infeccioso (politraumatizados). La similitud en la incidencia, severidad y secuencia de aparición de la falla en ambos grupos, pese a la diferencia en la presencia de infección asociada, lo hace concluir que la infección no es una condición indispensable para el desarrollo de este evento. Y planteó además que existía una activación masiva de mediadores de la inflamación como consecuencia del dańo tisular.
Un ańo mas tarde el mismo Goris10 es capaz de inducir cuadros de "sepsis" y fallo multiorgánico mediante la inyección de Zymosán intraperitoneal en animales de experimentación (sustancia química que activa el sistema del complemento y subsecuentemente toda la cascada inflamatoria), en ausencia de infección.
Con el objetivo de unificar criterios y conceptos, en 1991 el American Collage of Chest Physicians and Society of Critical Care Medicine (ACCP/SCCM) reunidos en la Conferencia de Consenso de Chicago lo definen,11 para beneficio nuestro.
DEFINICIÓN.
Así el término disfunción de órganos nace como resultado de la Conferencia de Consenso de la ACCP/SCCM11, al reconocer que los criterios para determinar la existencia de un trastorno de la función de un determinado órgano ó sistema, es un proceso continuo y dinámico y no un fenómeno dicotómico como el concepto de falla orgánica, que además de ser arbitrario es tardío en su diagnóstico y los criterios utilizados son diferentes de un estudio a otro.
Es la disminución potencialmente reversible en la función de uno o más órganos, que son incapaces de mantener la homeostasis sin un sostén terapéutico. El término disfunción implica un proceso continuo y dinámico en la pérdida de la función de un órgano, que va de menos a más, siendo la etapa final en la claudicación de la función de dicho órgano lo que denominamos falla.
El Síndrome de Disfunción Orgánica Múltiple (SDOM) se considera como un conjunto de síntomas y signos de patrón diverso, que se relacionan en su patogenia, están presentes por lo menos durante 24 a 48 horas y son causados por disfunción orgánica, en grado variable, de dos o más sistemas fisiológicos, con alteración en la homeostasis del organismo, y cuya recuperación requiere múltiples medidas de soporte avanzado12.
Asimismo debemos definir el SDOM primario cuando ocurre una vez que cualquier sistema orgánico falla, en forma evidente o sea como resultado directo de una lesión conocida, por ejemplo, luego de un episodio de insuficiencia respiratoria aguda por lesión pulmonar después de un trauma tisular global o contusión pulmonar, la insuficiencia renal aguda por rabdomiólisis y a la coagulopatía por politransfusión. El SDOM secundario es el que se presenta en el contexto de una respuesta inflamatoria sistémica, o consecuencia de la respuesta del huésped a una agresión englobándose en el Síndrome de Respuesta Inflamatoria Sistémica (SRIS), es el nexo que media entre la injuria (infecciosa o no) y el SDOM13.
El SRIS y el SDMO son la vía final común de muerte en pacientes severamente enfermos o lesionados, en los que la tecnología avanzada existente en las UCI ha posibilitado su resucitación.
DEFINICIÓN DE LAS DISFUNCIONES ORGÁNICAS.
Son varios los órganos y sistemas que están expuestos al riesgo de entrar en disfunción, en pacientes en estado crítico, dentro de los más propensos descritos en la literatura14-19 están: respiratorio, renal, cardiovascular, neurológico, hepático y hematológico. No existen criterios uniformes para definir la insuficiencia o disfunción de un órgano determinado, pues la mayoría de los autores utilizan su propia terminología y parámetros, lo que ańade confusión a un campo ya complejo. Consideramos oportuno mostrar algunos de los mismos para tener una idea de magnitud del problema.
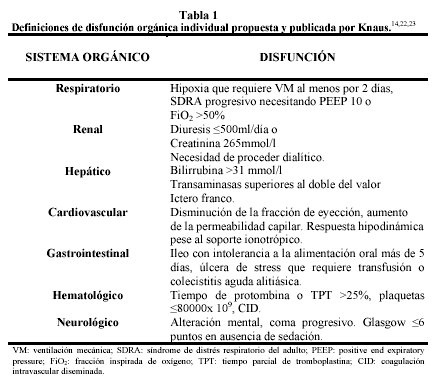
Siete sistemas definen al SDOM en más de la mitad de 30 publicaciones revisadas, entre los ańos 1969 al 1993, por Marshall20 coincidiendo con los criterios de Knaus14y Deitch17 (Tabla 1).
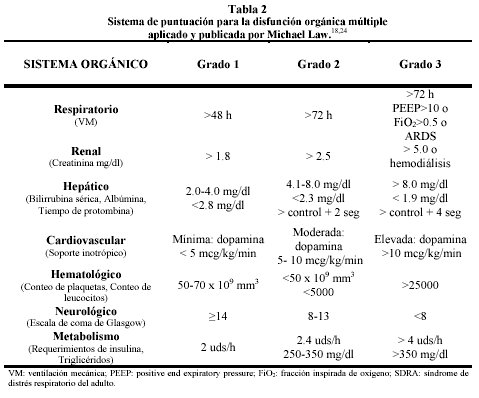
En 1994, Michael M Law18 expone su índice en el cual se evaluaron los sistemas pulmonar, renal, hepático, cardíaco, gastrointestinal, hematológico, neurológico y endocrino. La puntuación individual de cada órgano fue sumado en cada paciente, calculándose el Índice de Disfunción Orgánica Múltiple (IDOM), que podría llegar desde 0 hasta 24 puntos. La DOM fue definida cuando el IDOM era de 8 puntos o más (Tabla 2).
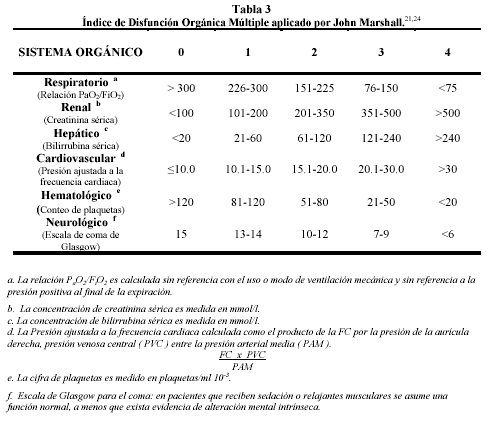
En 1995 John Marshall con su Índice de Disfunción Orgánica21 revolucionó los criterios sobre el tema al considerar por medio de un mecanismo de puntuación, la magnitud de la disfunción de cada uno de los 6 sistemas orgánicos analizados, otorgándoles un valor entre 0 y 4 según la magnitud de la disfunción. Este sistema de puntuación se correlacionó estrechamente con la mortalidad intra UCI tanto cuando se utilizaban los valores obtenidos durante las primeras 24 horas desde la admisión como cuando se aplicaba durante la estadía (valores bajo curvas ROC de 0.936 para la población analizada y de 0.928 para el grupo de validación). (Tabla 3). Los tres índices descritos han sido utilizados en estudios realizados en nuestro hospital y que serán comentados en la segunda parte de este trabajo22-25.
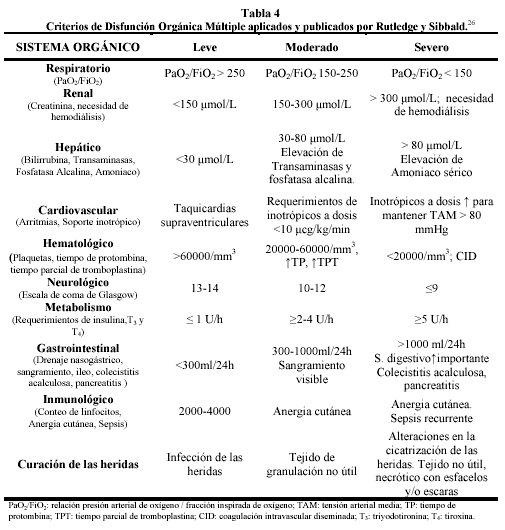
Aunque en la actualidad generalmente se excluye al sistema gastrointestinal, debido a la ausencia de un adecuado parámetro que describa el grado de disfunción o fallo en puntuaciones Rutledge y Sibbald26 lo incluyen en su investigación, junto a otras disfunciones como la inmunológica y la curación de las heridas, coincidiendo con los criterios de Bazzota27, ambas referencias categorizan también a las disfunciones como leve, moderada y severa lo que representando un método más sensible de reconocer la progresión de la disfunción al fracaso (Tabla 4).
Jean Roger Le Gall, en 1996, desarrolló un nuevo Índice de Disfunción Multi Orgánica28 (LOC), analizando 6 sistemas con una mayor posibilidad de parámetros para cada uno de ellos. Al igual que el índice de Marshall otorga una puntuación según la severidad de la disfunción de un sistema orgánico pero otorga además un valor relativo a la disfunción existente según sea el órgano o sistema comprometido.
Jean Louis Vincent y cols con su versión Europea de los Índices de Disfunción (SOFA), no agrega cambios conceptuales significativos a los sistemas anteriores pero los hace clínicamente más amigables29 (Tabla 5).
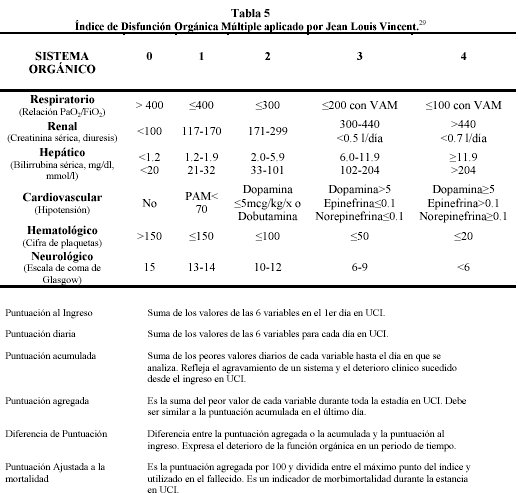
Una de las mayores utilidades de estas puntuaciones, independiente de cual se use y las pequeńas diferencias que entre ellos existan, es que nos permiten hacer un pronóstico objetivo sobre la evolución del paciente. En la práctica clínica, cuando tenemos más de tres órganos en falla por más de 48 horas, la mortalidad se eleva por sobre el 90%, debiendo plantearse seriamente y con la familia la posibilidad de limitar el tratamiento en curso.
En nuestro país se han utilizado criterios simplificados como lo reporta Elias Bécquer30 considerando a la insuficiencia orgánica como un espectro de alteraciones con diferentes grados de severidad, en los que hay que tener en cuenta el curso, dado que el grado de disfunción puede variar con el tiempo. Considerando que el paciente debe tener las alteraciones orgánicas por un periodo de 24 horas o mayor y que éstas no deben depender de una afección crónica previa.
FACTORES PREDISPONENTES.
Son múltiples los factores de riesgo o predisponentes relacionados con el desarrollo del SDOM que pueden contribuir a la aparición de alteraciones en el proceso de respuesta ante las agresiones26,30,31. Frecuentemente un paciente evidencia varios de ellos al mismo tiempo. Los factores más comúnmente encontrados son:
Factores de riesgo
-
1. Reanimación retrasada o inadecuada.
2. Foco infeccioso o inflamatorio persistente.
3. Presencia de hematomas.
4. Edad de 65 ańos o más.
5. Disfunción orgánica previa.
- a) Enfermedad renal con uremia.
b) Enfermedad respiratoria crónica (obstructiva o restrictiva).
c) Insuficiencia cardiaca congestiva.
d) Enfermedad hepática.
- a) Diabetes.
b) Alcoholismo.
c) Malnutrición.
d) Cáncer.
e) Tratamiento con esteroides.
f) Tratamiento con citostáticos.
g) SIDA.
ETIOLOGÍA.
Inicialmente se pensó que éste cuadro era la expresión fatal de una sepsis incontrolada, sin embargo posteriormente se ha demostrado que puede ocurrir en ausencia de infección.
La incidencia del SDOM en una población de pacientes hetereogénea ó mixta (patologías de tipo médico y quirúrgico) varía entre 7 y 15% 12,19,21,26,32. En pacientes con trauma su incidencia puede ser hasta del 35%, y mucho menor en pacientes luego de cirugía cardíaca electiva, alrededor del 3%.
Es difícil encontrar un elemento causal simple para el SDMO, existiendo en la mayoría de los pacientes varias causas que se potencian o sinergizan.
1. Traumatismos multisistémicos graves.
2. Postoperatorio.
3. Inestabilidad hemodinámica.
4. Infecciones severas.
5. Pancreatitis aguda.
6. Quemados.
7. Necesidad de ventilación mecánica prolongada.
8. Hemorragia gastrointestinal.
9. Disección, ruptura o reparación de aneurisma aórtico.
10. Perforación gastrointestinal.
11. Enfermedad inflamatoria intestinal.
12. Nutrición parenteral prolongada.
13. Cirugía valvular cardiaca.
14. Transfusiones masivas.
15. Coagulación intravascular diseminada.
FISIOPATOLOGÍA.
Hasta la fecha gran cantidad de estudios clínicos y de laboratorio han acumulado suficiente evidencia de la existencia de una participación activa de la cascada inflamatoria en la génesis de cuadros de disfunción orgánica múltiple. Es así como noxas de origen infeccioso ó no infeccioso son capaces de iniciar el proceso inflamatorio, activando vías comunes que a manera de respuesta inespecífica, permiten al huésped reaccionar frente a la injuria
Los mecanismos de producción del SRIS y SDMO son complejos e interrelacionados y no están todavía totalmente aclarados. Las alteraciones se producen a partir de un evento inicial o agresión que produce como respuesta la activación de complejas cascadas humorales y celulares que van dirigidas inicialmente a controlar la situación, pero se hacen excesivas e incontroladas provocando una respuesta inflamatoria generalizada que conduce a dańo capilar, aumento de la permeabilidad vascular, edema intersticial, alteraciones microcirculatorias y finalmente Disfunción e insuficiencia orgánicas19,33.
Así se presentan los principales aspectos fisiopatológicos del SDOM (Figura 1):
- A. Respuesta normal del huésped a la agresión (estrés).
B. Patogénesis: hipótesis
Existen varias hipótesis para explicar la iniciación y desarrollo de la respuesta inflamatoria sistémica y el SDOM que tienen múltiples aspectos imbricados entre sí. Con el fin de lograr una mejor comprensión de las mismas vamos a desarrollarlas separadamente, pero debemos tener siempre presente que estos mecanismos tienen gran número de aspectos comunes y superpuestos.
Históricamente, la sepsis se ha planteado como la causa de este síndrome, hipótesis infecciosa. Su presencia se consideró requisito indispensable para realizar su diagnóstico. Sin embargo, en los ańos 80 se evidenció que en gran parte de los casos no se constataron focos sépticos clínicamente ni en las necropsias y aunque se detectara y drenara un absceso no siempre se revertía en el SDOM, lo que ha sugerido que el complejo SRIS-SDOM no necesita de un foco infeccioso para mantenerse13.
Posteriormente se desarrollo la teoría "intestinal" o "de translocación bacteriana", que aboga por la migración de bacterias y endotoxinas del intestino a la sangre y la producción de sepsis y SDOM. Hay evidencias de que en diferentes enfermedades humanas ocurre la translocación bacteriana, que puede provocar un desequilibrio en mediadores de la inflamación34-36.
Principales aspectos fisiopatológicos del SDOM
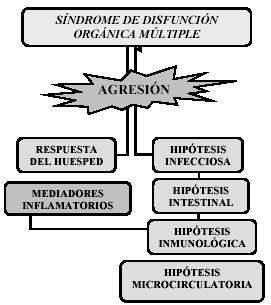
Más recientemente, y apoyada en la identificación de mecanismos relacionados con el SRIS y el SDOM se ha planteado la hipótesis inmunológica que explica el desarrollo de estos síndromes a partir de la intensa y prolongada estimulación de los macrófagos y los linfocitos, con la subsecuente producción y liberación excesiva de citoquinas. Esta teoría destaca que independientemente de una infección, una lesión inicial (1er golpe) impacta y prepara los mecanismos inflamatorios en un proceso predominantemente subclínico en su inicio, y una segunda agresión (2do golpe) desencadena la liberación de mediadores en una respuesta inflamatoria exagerada ya en el ámbito clínico, que conduce a la DOM19,37.
Por último la hipótesis microcirculatoria propone que la disfunción orgánica se debe a la lesión microcirculatoria generalizada ocasionada por la entrega inadecuada de oxígeno a nivel tisular, el fenómeno de "reperfusión" y las interacciones entre el endotelio y los leucocitos38,39.
A. Respuesta normal del huésped a la agresión (estrés).
El organismo humano responde ante una agresión determinada (hipoxia, trauma, hemorragia, infección, etc.) liberando substancias de diferente origen y composición química, conocidas genéricamente como "mediadores" los cuales actuar localmente y a distancia, y promueven una respuesta de los diferentes sistemas y órganos con el fin de limitar la lesión inicial, y favorecer su reparación y recuperación.
Los mediadores se consideran primarios cuando están previamente preformadas dentro de la célula, usualmente formando gránulos, listos para ser expulsados ante determinados estímulos y secundarios cuando solo se sintetizan, una vez la célula es estimulada, liberándose en forma inmediata. Actúan a nivel endocrino (a distancia, en tejidos diferentes al que se producen, circulando en la sangre, en cantidades muy variables), paracrino (en células vecinas) y autocrino (en la célula que las produce) (Figura 2).
Respuesta normal del huésped a la agresión (estrés).
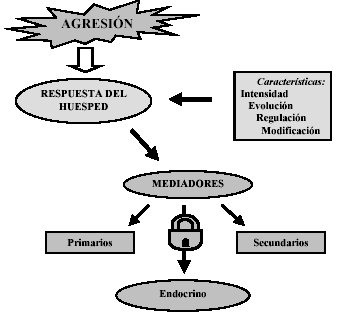
La respuesta al estrés tiene algunas características generales:
-
1. Su intensidad, proporcional a la severidad de la lesión inicial, a la lesión producida y a la presencia de factores concomitantes que perpetúan el estímulo. La respuesta máxima ocurre 3 a 5 días después del estímulo inicial, disminuyendo progresivamente hasta desaparecer en los casos no complicados entre los 7 y 10 días.
2. Evolución en fases: inicial o de sufrimiento celular caracterizada por hipoperfusión, disminución del metabolismo, del consumo de oxigeno, de la temperatura corporal y de la presión arterial que dura varias horas y fase secundaria que incluye un período de respuesta de la fase aguda en el cual se incrementan los mediadores y proteínas de la fase aguda; hay hipermetabolismo y catabolismo y un período de adaptación en el cual predomina el anabolismo, disminuyen los mediadores y el hipermetabolismo, hay restauración de las proteínas viscerales y cicatrización de las lesiones y dura varias semanas.
3. Regulación: Está regulada por varios sistemas, destacándose el, llamado eje neuro-inmuno-endocrino y el sistema hepático-muscular, los cuales ejercen sus efectos por medio de hormonas y citoquinas.
4. Modificación: Puede ser modificada por múltiples factores de ocurrencia frecuente en los pacientes hospitalizados tales como: factores que incrementan la respuesta: catecolaminas, hormona tiroidea, dolor, inanición, insomnio, infección, complicaciones quirúrgicas o de tipo médico, actividad motora, agitación psíquica, desacoplamiento de la fosforilación oxidativa y en el ciclo de Krebs, metabolismo ineficiente a través del ciclo de Cori o por anaerobiosis. Y factores que disminuyen la respuesta: prostaglandinas, sedantes y analgésicos, relajantes neuromusculares, alfa y beta bloqueadores, sepsis en estado terminal.
B. Patogénesis: hipótesis
Hipótesis Infecciosa.
El SDOM inducido por la infección (sepsis severa), no es secundario a la acción directa de las bacterias, sino es debido a la acción de los mediadores de la inflamación producidos por el propio paciente. Actualmente se acepta que la DOM de la sepsis severa es la manifestación de una lesión endotelial generalizada, que se observa en el contexto de una respuesta excesiva y descontrolada de los mediadores de la inflamación, los que normalmente son liberados frente a la agresión de microorganismos invasores (Figura 3).40-43
Relación entre el síndrome de respuesta inflamatoria sistémica y síndrome de respuesta anti-inflamatoria compensadora en sepsis grave.
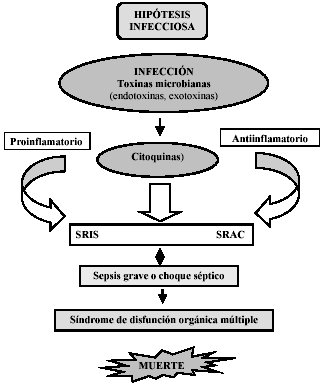
En la fase inicial de la respuesta a la infección, la liberación de endotoxinas o exotoxinas por las bacterias induce la activación de macrófagos, los que sintetizan y liberan citocinas proinflamatorias que provocan cambios a nivel endotelial y modifican el equilibrio procoagulante-anticoagulante, proceso que evoluciona a la obstrucción y mal funcionamiento de la microcirculación con disfunción orgánica44.
La respuesta inflamatoria en la infección es mediada por las citocinas las cuales son péptidos inmunorreguladores que interactúan sobre receptores localizados en diferentes líneas celulares. Esta respuesta guarda un estrecho equilibrio que es mediado por citocinas proinflamatorias y antinflamatorias:
Citocinas proinflamatorias:
Citocinas antiinflamatorias:
De acuerdo a la intensidad del disparador inicial y de la relación entre ambas respuestas el Dr. Roger Bone ha descrito varias fases evolutivas:
En las dos primeras se llega al equilibrio inmunológico, pero cuando sale del control evoluciona a un desequilibrio en el que predomina el SRIS o hay bloqueo inmunológico grave que lleva al enfermo a la DOM e infección no controlada como se presenta en la disonancia inmune y parálisis inmunológicas.
Por eso hoy unánimemente es aceptado el concepto referido por Lewis Thomas en los comienzos del '70 cuando decía: …"es nuestra propia respuesta a la presencia de bacterias siendo la causante de la enfermedad"45.
Hipótesis Intestinal:
La translocación bacteriana que constituye el paso de las bacterias (bacteriemia endógena) y sus productos, endotoxinas, (sepsis abacteriémica) a través de la mucosa gastrointestinal ayuda a explicar la aparente paradoja entre la no localización de un foco séptico y aparición del SDOM. Para que se produzca esta translocación debe haber una isquemia de la mucosa y ruptura de la barrera intestinal. Este paso induce la activación del sistema inmune inflamatorio local y de las células de Kupffer en el hígado con producción de mediadores que exacerban la respuesta inflamatoria sistémica y provocan una mayor permeabilidad intestinal, lo que lleva a un círculo vicioso. Por lo que se ha planteado que si el sistema inmune es el "motor" de la DOM, el intestino es el "pistón" de dicho "motor"13,35,46.
Existen varios factores implicados:
1. Alteraciones de la flora bacteriana gastrointestinal
2. Alteración de los mecanismos defensivos locales del huésped.
3. Lesión anatómica y funcional de la mucosa intestinal.
Hipótesis Inmunológica.
Se ha logrado identificar numerosos elementos y mediadores de la respuesta inflamatoria implicados. La estimulación de los macrófagos y los linfocitos, con la subsecuente producción y liberación excesiva de citoquinas (IL-1, IL-2, IL-5, IL-6, IL-8) las cuales, en condiciones usuales, tienen acciones benéficas para el organismo sobre el metabolismo intermediario, la cicatrización de las heridas, la inducción de la respuesta de la "fase aguda", la producción de fiebre y otros procesos a nivel cardiovascular, respiratorio, renal y hepático. Se convierten en substancias nocivas cuando se alteran los mecanismos de control que regulan la respuesta inflamatoria, por diversas razones con incremento de las substancias pro-inflamatorias (FHT, IL-1, IL-2, IL-5, IL-8, FAP) y disminución de las anti-inflamatorias (IL- IRA, IL- lo, RFNT, esteroides, catecoles) Esta teoría tiene gran número de aspectos comunes y superpuestos con las otras44.
Hipótesis microcirculatoria.
Propone que la disfunción orgánica se debe a la lesión microcirculatoria generalizada ocasionada por la entrega inadecuada de oxígeno a nivel tisular, el fenómeno de "reperfusión" y las interacciones entre el endotelio y los leucocitos ante la respuesta exagerada, en contraste a una respuesta coordinada, controlada y beneficiosa para el huésped en situación normal, lleva a una alteración de la permeabilidad capilar, con trastornos de la microcirculación, alteraciones de la coagulación y del metabolismo celular, la fase inicial de la respuesta a la infección.45,47
A. Isquemia.
La hipoxia celular conlleva una sede de cambios ("hypoxic priming") dentro de las cuales están:
a. Edema celular: por disminución en la actividad de la sodio-potasio ATPasa, se presenta acúmulo de sodio y agua intracelular
b. Estimulación de los sistemas de segundo mensajero. Hay acúmulo de calcio intracelular e incremento en los niveles de AMP cíclico
c. Se lesiona el endotelio vascular por diferentes mecanismos (acidosis intracelular, acúmulo de calcio intracelular, pérdida de precursores del ATP y producción de radicales libres de oxígeno)
d. Disminución de los mecanismos antioxidantes
e. Se modifica la expresión genética de las proteínas de respuesta al estrés (proteínas heat shock, proteínas de respuesta oxidativa, proteínas de fase aguda)
B. Reperfusión.
El re-establecimiento del flujo sanguíneo luego de un período de isquemia, desencadena el denominado "fenómeno de reperfusión" el cual por si solo ocasiona lesión tisular. En este proceso juega un papel fundamental la producción excesiva de radicales libres a partir de los polimorfonucleares (NADPH oxidasa), de la célula endotelial y los tejidos (xantinoxidasa, endoperóxido cíclicos, autooxidación de catecolaminas). Hay órganos particularmente sensibles como el tracto gastrointestinal, el hígado, el rińón y el pulmón. Los radicales libres lesionan la membrana celular, los organelos, degradan las proteínas y causan disrrupción de los cromosomas.
C. Interacciones célula endotelial-leucocitos.
La reperfusión tisular estimula la inflamación por activación de polimorfonucleares y plaquetas, agrava la lesión endotelial y ocasiona un desequilibrio en la producción de las substancias vasoactivas (endotelinas, óxido nítrico), las sustancias procoagulantes (inhibidor del plasminógeno, factor V, factor de activación plaquetario, fibronectina), las anticoagulantes (prostaciclina, trombomodulina, proteínas C y S), los factores de adhesión intercelular (ICAM-1, ICAM-2, ELAM-1) y las citoquinas (IL-1,IL).
Apreciamos así que el enfoque propuesto por diferentes autores12,15,19,30,41 es sistémico, máxime cuando se trata del organismo humano considerado la expresión mayor de la perfección sistémica.
CONCLUSIONES.
Cuando un factor causal desata en el organismo una respuesta inmediata, fundamentalmente inmunológica, que se hace sistémica, liberándose productos que ocasionan lesiones endoteliales y anóxicas en diversos órganos, estamos en presencia del Síndrome de Disfunción Orgánica Múltiple.
Como evento de gran importancia y reto en la vida del intensivista constituye la vía final que ocasiona la muerte a muchos de los pacientes hospitalizados en los servicios de cuidados intensivos, particularmente en pacientes quirúrgicos complicados, politraumatizados o con sepsis. Demandando de altos costos de hospitalización y rehabilitación y ejerciendo notorio impacto familiar y social así como en el personal médico y de enfermería
Aunque existen múltiples criterios para definirlo su presencia generalmente es válida cuando ante un factor causal se constata disfunción en 3 o más órganos Varias causas han sido relacionadas y generalmente se encuentran en asociación, se potencian o sinergizan.
La incidencia, factores predisponentes, evolución y pronóstico, obtenidos del análisis de series de pacientes varían entre los estudios siendo innumerables los órganos y sistemas que están expuestos a la disfunción o son más vulnerables en los enfermos críticos, por lo general los más afectados son el respiratorio, el cardiovascular (con mayores porcentajes), el hígado y los rińones.
Los aspectos epidemiológicos y pronósticos son comentados en la segunda parte de esta trabajo, donde son contrastados los estudios locales sobre el pronóstico con los resultados internacionales.
REFERENCIAS:
1. Carrico CJ, Meakins JL, Marshall JC. Multiple organ failure syndrome. Arch Surg 1986; 121:196-208.
2. Rabell S, Gutiérrez FN, Ruibal A, Lino P, Valdés J. La falla multiorgánica. Revisión del síndrome. Unidad de Cuidados Intensivos "Hospital Calixto García" 1991; 1-63.
3. Ibáńez J, Raurich JM. El fracaso multiorgánico. En: Net A, Mancebo J, Benito S, editores. Shock y fallo multiorgánico. Barcelona: Springer-Verlang Ibérica; 1992. p. 143-8.
4. Tilney Nl, Bailey GL, Morgan AP. Sequential systems failure after rupture of abdominal aortic aneurysms: An unsolved problem in postoperative care. Ann Surg 1973; 178: 117-22.
5. Baue AE. Multiple, progressive or sequential systems failure. A syndrome of the 1970s. Arch Surg 1975; 110: 779-81.
6. Fry DE, Perlstein L, Fulton RL, Polk HC. Multiple system organ failure: the role of uncontrolled infection. Arch Surg. 1980; 115: 136-42.
7. Bozotta A, Polk HC. Insuficiencia múltiple de órganos. Clin Quir Norteam 1983; 2: 311-22.
8. Barzilay E, Kessler D, Berlot G. Use of extracorporeal support techniques as aditional treatment for septic-induced multiple organ failure patient. Crit Care Med 1989; 17:634-37.
9. Goris RJ, Boekhorst TAP, Nuytinck JKS, Gimbrere JSF. Multiple organ failure. Generalized autodestructive inflammation? Arch Surg 1985; 120: 1109-15.
10. Goris RJ, Boekhorst TAP, van Bebber JP. Multiple organ failure and sepsis without bacteria. Arch Surg 1986; 121: 897-901.
11. Bone R, Balk R, Cerra, Dellinger RP, Fein AM, Knaus A et al. American College of Chest Physicians/ Society of Critical Care Medicine Consensus Conference: Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Crit Care Med 1992; 20: 864-74.
12. Correa H. Sepsis, disfunción orgánica múltiple y shock: aspectos clínicos. En: Castro J, Hernández G. Sepsis y falla multiorgánica. 2da ed. Santiago, Chile: Ed. Mediterranio, 1999; 47-60.
13. Morlans K, Santos J, González-Prendes CM, Rodríguez F, García B, Saínz H. Falla Orgánica Múltiple: Acercamiento al tema. Rev Cubana Cardiol Cir Cardiovasc 1999; 13: 61-71.
14. Knaus WA, Draper EA, Wagner EP. Prognosis in acute organ system failure. Ann Surg 1985; 202: 685-692.
15. Deitch EA. Multiple organ failure. Pathophysiology and potential therapy. Ann Surg 1992; 216: 117-134.
16. Bone RC. Fracaso Multiorgánico y sepsis. Hospital Practice 1992; 7: 43-52
17. Deitch EA. Multiple Organ Failure. Advances in Surgery 1993; 26: 333-35.
18. Law MN, Cryer HG, Abraham E. Elevated levels of soluble incam-1 correlate with the development of multiple organ failure in severely injured trauma patients. J Trauma 1994; 37: 100-110.
19. Moore FA, Moore EE. Conceptos en evolución sobre la patogenia de la insuficiencia orgánica múltiple después de traumatismo. Clin Quirur Norteam 1995; 2: 237-54.
20. Marshall JC: Descriptors of organ system dysfunction for the multiple organ dysfunction syndrome (MODS). In: Clinical Trials for the Treatment of Sepsis. Sibbald WJ, Vincent JL, editors. Berlin, Springer-Verlag, 1995, 122-138.
21. Marshall JC, Cook DJ, Christou NV, Bernard GR, Sprung CL, Sibbald WJ. Multiple Organ Dysfunction Score: A reliable descriptor of a complex clinical outcome. Crit Care Med 1995; 23: 1638-52.
22. López SC, Iraola MD, Álvarez FC, Dávila E, Álvarez MC. Factores de riesgo para la mortalidad de los pacientes quirúrgicos en la unidad de cuidados intensivos. Rev Esp Anest Rean 2000; 47: 281-286.
23. Iraola MD, Nieto PR, Álvarez FC, Pons F, Cruz H. Síndrome de Respuesta Inflamatoria Sistémica: morbilidad y mortalidad en pacientes quirúrgicos ingresados en la unidad de cuidados intensivos. Rev Cub Med Int Emerg 2003; 2: 35-43.
24. Olivera D, Iraola MD, Alvarez FC, Nieto PR, Aguila O. Factores pronósticos para la mortalidad en la peritonitis. Rev Portuguesa de Cuidados Intensivos 2000; 9:217-220.
25. Misas M, Iraola MD, Álvarez F, Nieto PR, Pons F. Índice de disfunción orgánica múltiple en pacientes quirúrgicos ingresados en la unidad de cuidados intensivos. Rev Cub Med Int Emerg 2003; 2: 35-44.
26. Rudledge FS, Sibbald WJ. Multiple organ system failure: a spectrum of risk and of disease. In: Sivak ED, Higgins TL, Seiver A, editors. High Risk Patient: Management of the Critically Ill. Baltimore, MD: Williams and Wilkins 1995: 1291-1312.
27. Bazzota AP, Polk HC. Multiple system organ failure. Surg Clin North Am. 1997; 63: 315-6.
28. Le Gall JR, Klar J, Lemeshow S y cols. The Logistic Organ Dysfunction System. A new way to assess organ dysfunction in the intensive care unit. ICU scoring group. JAMA 1996; 276: 802-10.
29. Vincent JL, de Mendonca A, Cantraine F, Moreno R, Takala J, Suter PM, et al. Working group on "sepsis-related problems" of the European Society of Intensive Care Medicine. Use of the SOFA score to assess the incidence of organ dysfunction/failure in intensive care units: results of a multicenter, prospective study. Crit Care Med 1998; 26: 1793-800.
30. Bécquer E. Síndrome de disfunción múltiple de órganos. En: Caballero A, editor. Terapia Intensiva. 2000. 5251-5316.
31. Sauaia A, Moore FA, Moore EE. Early risk factors for postinjury multiple organ failure. World J Surg 1996; 20: 392-400.
32. Hotchkiss RS, Karl IE. The fas death pathway as a mechanism of multiple organ disfunction syndrome: Not so fast. Crit Care Med 2001; 29: 901.
33. Nakatani T, Kobayashi K. Surgical stress and organ dysfunction: Liver. J Japan Surg Soci 1996; 97:752-58.
34. Romaud JA. Bacterial translocation in the critically ill. Current Opinion in Crit Care 1996; 2: 371-74.
35. Swank GM, Deitch EA. Role of the gut in multiple organ failure: Bacterial translocation and permeability changes. World J Surg 1996; 20:411-17.
36. Lemaire LC, Lanschot JJ, van Stoutenbeeck CP, Deventer SJ, van Wells CL, Gouma DJ. Bacterial translocation in multiple organ failure: cause or epiphenomenon still unproven. Br J Surg 1997; 84: 1340-50.
37. Schlag G, Redl H. Mediators of injury and inflammation. World J Surg 1996; 20:406-10.
38. Bone RC: Immunologic dissonance: a continuing evolution in our understanding of the systemic inflammatory response syndrome (SIRS) and the multiple organ dysfunction syndrome (MODS). Ann Intern Med 1996; 125: 680-7.
39. Sharma S, Eschun G. Multisystem Organ Failure of Sepsis. 2003, eMedicine.com, Inc. 1-25
40. Carrillo R, González JA. Inflamación-endotelio-coagulación en sepsis. Conceptos actuales. Cir Ciruj 2002; 70: 433-44.
41. Balk RA. Patogenesis and management of multiple organ dysfuntion or failure in severa sepsis and septic shock. Crit Care Clin 2000; 16: 337-352.
-
Correspondencia:
Dr. Marcos D. Iraola Ferrer
Avenida 52, Número 6501-B, Entre 65 y 67. CP: 55200. Cienfuegos 2. Cuba
Tel: 053-432-519202
Fax: 053-432-517387
E-mail: mif @ gal.sld.cu
