Indice del volumen
Volume index
Comité Editorial
Editorial Board
Comité Científico
Scientific Committee
- 1.- Apnea:
- 1.a.-Apnea Obstructiva: Ausencia de flujo oro-nasal de cualquier duración con persistencia de esfuerzo respiratorio
- 1.b.- Apnea Central: Ausencia de flujo oro-nasal de al menos 20 segundos de duración que se acompańa de ausencia de esfuerzo respiratorio o menores de 20 segundos si se acompańan de arousal, desaturación o bradicardia.
- 1.c.- Apnea Mixta: Ausencia de flujo oro-nasal con un componente central y un componente obstructivo.
- 2.- La Hipopnea en el nińo, se define como una reducción del 50% o más de la amplitud de la seńal de flujo oro-nasal, medido con termístor, durante al menos el tiempo equivalente a dos ciclos respiratorios, con persistencia del esfuerzo respiratorio, acompańado de desaturación mayor o igual del 3% y/o arousal. Si utilizamos la cánula de presión nasal, la hipopnea se define como cambio discernible en la onda de flujo de al menos el tiempo equivalente a dos ciclos respiratorios, con persistencia de esfuerzo respiratorio, acompańado de desaturación mayor o igual del 3% y/o arousal.
- 3.- RERA (Esfuerzo Respiratorio Relacionado con Arousal): Evidencia de aumento del esfuerzo respiratorio o limitación al flujo aéreo que finaliza con un arousal, seguido de la normalización del esfuerzo respiratorio y del flujo aéreo.
- 4.- Limitación al flujo: Aplanamiento de la rama inspiratoria de la onda de flujo de la cánula nasal
- 5.- Hipoventilación:
- 5.1.- Hipoventilación obstructiva: Valores de dióxido de carbono espirado (PETCO2)> 50 mmHg durante> 10% del tiempo total de sueńo (TST), o valores pico de PETCO2> 53 mmHG, acompańándose de respiración paradójica o eventos obstructivos.
- 5.2.- Hipoventilación Central: presencia de cifras de PETCO2 > 50 mmHG durante > 10% del TST o PETCO2 pico > 53 mmHG, acompańándose de un descenso del esfuerzo respiratorio
- 6.- Respiración periódica: Sucesión de tres o más apneas centrales de al menos tres segundos de duración separadas por menos de 20 segundos de respiración normal
- 1.- Alteraciones nasales, con disminución del calibre de paso de aire: estenosis o atresia de coanas, desviación de tabique septal, poliposis nasales
- 2.- Alteraciones en nasofaringe:
Hipertrofia adenoamigdalar, macroglosias, higroma hístico, cirugía del paladar hendido. Especial mención merece la hipertrofia adenoamigdalar, puesto que en la edad infantil supone la causa más frecuente de SAHS16, aproximadamente las tres cuartas partes de las series publicadas. Aunque no todos los nińos con hipertrofia adenoamigdalar padecen SAHS, la presencia de hipertrofia adenoamigdalar aumenta la incidencia del SAHS en estas edades de la vida.
Los procesos infecciosos de vías altas repetidos, pueden agravar SAHS leves o desencadenar su desarrollo en la infancia al producir hipertrofia del tejido linfoide faringoamigdalar. - 3.- Alteraciones craneofaciales:
Micrognatia maxilar superior, micrognatia mandibular y/o retrognatia, hipoplasia mandibular, hipoplasia mediofacial. Estas alteraciones esqueléticas suelen ir asociadas a síndromes malformativos como Síndrome de Pierre - Robin, Síndrome de Teacher - Collins, Síndrome de Down, Síndrome de Crouzon, Síndrome de Apert, entre otros, que hacen que en estas patologías aumente la incidencia de SAHS. - 1.- Hipotonía faríngea relacionada con el sueńo REM
- 2.- Control neurológico anómalo: hipotonía generalizada, alteraciones del SNC, alteraciones de tronco-encéfalo
- Las alteraciones del crecimiento, que podemos observar como manifestación clínica o como consecuencia de la presencia de un SAHS no tratado, parece que tiene un origen multifactorial:
- Déficit de ingesta calórica, aumento del gasto energético secundario a un aumento del esfuerzo respiratorio nocturno, alteraciones en la liberación de la hormona de crecimiento que tiene lugar durante las fases profundas de sueńo24. Algo muy importante, es que los nińos tratados de SAHS presentan un aumento del crecimiento pondero-estatural después del tratamiento.
- Aumento de la tensión arterial: en los nińos con índice de Apnea/Hipopnea (IAH) por hora de sueńo superior a 10, se ha observado un aumento de las presiones sistólicas y diastólicas tanto en vigilia como en sueńo REM25-28
- Alteración de la geometría y la estructura del ventrículo izquierdo, que mejora en los nińos con SAHS adecuadamente tratados29
- Alteraciones cognitivo-conductuales: La Odds ratio para
alteraciones neuroconductales en nińos roncadores es de 2.936. En los nińos con problemas respiratorios durante el
sueńo se multiplica por tres la frecuencia de alteraciones de conducta y problemas de atención. Las alteraciones del intercambio gaseoso nocturno pueden afectar al rendimiento escolar, de forma que los nińos con bajo rendimiento académico tienen más probabilidades de haber roncado durante la nińez temprana.
- Se ha sugerido la existencia de comorbilidad entre el síndrome de déficit de atención con hiperactividad (SDAH) y problemas respiratorios durante el sueńo, de forma que la Academia Americana de Pediatría recomienda que los nińos con presencia de hiperactividad y que no reúnan los criterios diagnósticos de SDAH deben recibir una exhaustiva evaluación de posible existencia de trastornos respiratorios del sueńo
- Enuresis nocturna, los nińos con SAHS tienen aumentada la producción de orina y la excreción salina, de manera que tienden a tener más micciones nocturnas20.
- 1.- Historia clínica completa, haciendo especial hincapié en la presencia de síntomas y/o signos relacionados con el sueńo.
- 2.- Exploración física completa con especial atención a la anatomía craneofacial y de las vías aéreas altas:
- 2.1.- Inspección del aspecto externo: La hipertrofia adenoamigdalar puede influir en el desarrollo de la hemicara inferior y mandibular al provocar respiración oral30,31, apareciendo la denominada facies adenoidea caracterizada por ojos hundidos, acumulo de secreciones en torno a las fosas nasales, boca abierta en reposo.
- 2.2.- Inspección del perfil: Para valorar las discrepancias maxilomandibulares, evidenciándose los casos de maloclusión dentoesquelética32.
- 2.3.- Exploración de cavidad oral y orofaringe, mediante inspección, valorando la hipertrofia amigdalar, graduándose de 0 a IV, en función del grado de obstrucción del espacio inter-amigdalino de 0% a 100%33.
- 2.4.- Radiografía lateral de cavum para partes blandas: Puede mostrarnos el tamańo de hipertrofia adenoidea30.
- 2.5.- Nasofibroscopia con endoscopio flexible, nos permite valorar: La permeabilidad de las fosas nasales, hipertrofia adenoidea, la existencia de atresia de coanas, las alteraciones laríngeas como la presencia de laringomalacia32.
- 3.- Estudio de sueńo nocturno: A este nivel existen diferentes técnicas diagnósticas, siendo la técnica de elección la polisomnografía nocturna (PSG)4,5 realizada en el laboratorio de sueńo.
- a.-Variables neurofisiológicas: Electroencefalograma, electrooculograma, electromiograma tibial y submentoniano. Permite la valoración de los estadios de sueńo y arquitectura de sueńo.
- b.-Variables cardiorrespiratorias con registro de:
- b.1.- Flujo oro-nasal: La medida de referencia de flujo aéreo es el neumotacógrafo que permite una medida cuantitativa del mismo, sin embargo, en la práctica clínica habitual lo más utilizado y aceptado como medida válida de flujo oro-nasal son los termosensores y más recientemente la utilización de cánulas nasales.
- b.2.- Esfuerzo respiratorio: Para clasificación de los eventos respiratorios en centrales, obstructivos o mixtos. La medida de presión esofágica mediante catéter esofágico constituye la técnica de referencia para medida de esfuerzo respiratorio, sin embargo, es una técnica agresiva y no bien tolerada, pudiéndose utilizar bandas piezoeléctricas torácicas y abdominales o pletismografía de impedancia.
- b.3.-Valoración del intercambio gaseoso:
- Saturación de oxigeno por pulxiosimetría,
- Medida del CO2 espirado o trascutáneo
- b.4.- Frecuencia cardiaca
- b.5.- Ronquido
- b.6.- Posición corporal
- SAHS persistente después de intervención quirúrgica
- SAHS asociado a otras patologías
- En el periodo prequirúrgico para estabilizar la vía aérea en nińos con aumento de riesgo quirúrgico.
SINDROME DE APNEAS/HIPOPNEAS DURANTE EL SUEŃO EN EDAD PEDIÁTRICA
Alonso Álvarez ML, Terán Santos J, Cordero Guevara J*,
Navazo Eguía A**, Coma del Corral MJ*.
Unidad de Trastornos Respiratorios del Sueńo. *Unidad de Investigación. **Servicio ORL.
Hospital General Yagüe. Complejo Asistencial de Burgos. Burgos, Espańa
mlalonso @ hgy.es
Rev Electron Biomed / Electron J Biomed 2006;2:89-99.
Comentario del revisor Dra. Marta Sofía López Rodríguez . Especialista en Anestesiología y Reanimación. Profesora Asistente del ISCMH. Facultad Finlay-Albarrán. Clínica Central Cira García Reyes. Habana. Cuba.
Comentario del revisor Dra. Patricia Muńoz Casas del Valle. Jefa del Departamento de Docencia, Investigación y Extensión Académica del Hospital Militar de Santiago. Santiago. Chile
Comentario de los revisores Dr. Claudio Rabec, Service de Pneumologie et Réanimation Respiratoire. Centre Hospitalier et Universitaire de Dijon. Dijon, France
y Dra. Vivian Leske, Laboratorio de Sueńo y Respiración. Servicio de Neurofisiología. Hospital Nacional de Pediatria "JP Garrahan". Buenos Aires, Argentina.
SUMMARY:
Sleep disordered breathing (SDB) is a common condition in children. Sleep Apnea/Hypopnea syndrome (SAHS) in children is a frequent sleep disorder, with a prevalence estimated to be 1 - 3% of all children. The most frequent cause of SAHS in children is the adenotonsillar hypertrophy. SAHS in children can result in severe complications if left untreated such as impaired physical growth, delayed development, poor school performance and in severe cases, hypertension and cor pulmonale, nevertheless, yet it is an under recognized condition. The gold standard diagnostic technique is the nocturnal polysomnography (PSG), guidelines for performing laboratory-based polysomnography in children have been established, the sleep laboratory should be a nonthreatening environment and personnel with pediatric training should record, score and interpret the study. The diagnostic criteria for SAHS in adults is not useful for diagnosis of SAHS in children. Adenotonsillectomy is the most common treatment for children with SAHS.
KEY WORDS: Sleep disordered breathing (SDB), Sleep Apnea/Hypopnea Syndrome in children (SAHS), children, Sleep studies
RESUMEN:
Los trastornos respiratorios del sueńo en los nińos, en particular el Síndrome de Apneas/Hipopneas durante el sueńo (SAHS), es una patología frecuente, que afecta entre el 1 - 3% de la población infantil, siendo su causa más frecuente la hipertrofia adenoamigdalar. Es una enfermedad infradiagnosticada y que conlleva importantes complicaciones como son alteraciones del crecimiento, alteraciones cognitivas e incluso en casos severos Cor Pulmonale. La polisomnografía nocturna (PSG), es la técnica diagnóstica de elección para el diagnóstico del SAHS en los nińos, pero en la población infantil es necesario tener en cuenta una serie de consideraciones, como son la edad de la población que se estudia, entorno adecuado y la necesidad de técnicos entrenados en el cuidado de los nińos. Los criterios diagnósticos del SAHS para adultos no son útiles en los nińos. El tratamiento de elección en los nińos con SAHS es la adenoamigdalectomia.
Palabras clave: Trastornos respiratorios de sueńo. Síndrome de apnea del sueńo. Nińos. Estudios de sueńo.
INTRODUCCIÓN
La primera descripción médica del Síndrome de Apneas / Hipopneas durante el sueńo (SAHS) se atribuye a William Osler en 18921, pero no fue hasta un siglo más tarde en 1972, cuando Guilleminault publicó la primera serie de nińos con SAHS2.
En general se habla de Trastornos Respiratorios del Sueńo, para abarcar un amplio abanico de patologías que van desde el ronquido, Síndrome de Resistencia Aumentada de la vía aérea superior, Síndrome de hipoventilación y Síndrome de Apneas / Hipopneas durante el sueńo, todas ellas caracterizadas por la presencia de alteraciones de la respiración durante el sueńo.
Se define el síndrome de Apneas /Hipopneas durante el sueńo (SAHS) en los nińos, como un trastorno de la respiración durante el sueńo caracterizado por una obstrucción parcial prolongada de la vía aérea superior y/o una obstrucción completa intermitente (apnea obstructiva) que altera la ventilación normal durante el sueńo y los patrones de sueńo normales. Se asocia con síntomas que incluyen ronquido habitual nocturno, dificultades con el sueńo y/o problemas de comportamiento. Las complicaciones pueden incluir alteraciones del crecimiento, alteraciones neurocognitivas y Cor Pulmonale, especialmente en los casos severos3-8.
DEFINICIONES:
Los criterios para valoración de trastornos respiratorios del sueńo utilizados en los adultos no son validos en los nińos5, 6. Recientemente han sido publicadas las definiciones de los diferentes eventos respiratorios en los nińos9:
PREVALENCIA
El ronquido es el síntoma más común de los nińos con SAHS, estimándose la prevalencia del ronquido entre un 10 - 12% 3,10-15. Es necesario diferenciar el denominado Ronquido simple no asociado a la presencia de apneas, ni alteraciones del intercambio gaseoso ni aumento de despertares nocturnos, del ronquido patológico asociado a la presencia de apneas.
La prevalencia del Síndrome de Apneas / Hipopneas durante el sueńo en los nińos de 4 - 5 ańos se estima entre 0,7% y 3% con un pico de incidencia máxima entre los 2 y 5 ańos10-15.
PATOGÉNESIS:
El nińo presenta una serie de
características anatómicas, fisiológicas y madurativas de la vía aérea superior (VAS) diferente del adulto. La edad pediátrica actualmente abarca desde neonatos hasta la adolescencia, aconteciendo durante ella el desarrollo, tanto físico como neurocognitivo y por tanto, está sujeto a un amplio número de factores patógenos que pueden modificar o alterar este proceso madurativo y de desarrollo normal.
En la patogenia del SAHS infantil influyen factores anatómicos y funcionales, de forma que el SAHS pediátrico es el resultado de la combinación de estos factores y no únicamente de un único factor.
Factores anatómicos:
Factores funcionales:
En resumen la patogenia del SAHS infantil es una conjunción de factores anatómicos y funcionales que llevan a un desequilibrio de la VAS traducido en colapso de la VAS y por tanto alteración de la respiración y de la ventilación normal durante el sueńo17.
CLINICA:
Las manifestaciones clínicas del SAHS infantil difieren del adulto18-20 (Tabla 1)
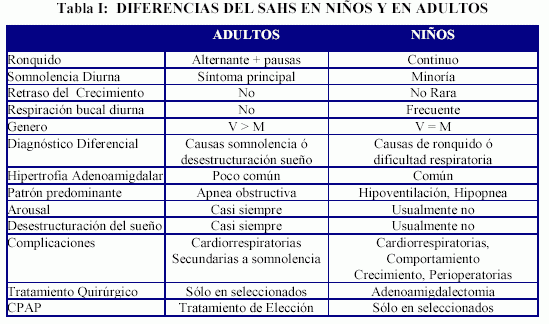
Las manifestaciones o signos clínicos del SAHS en la infancia son fundamentalmente nocturnos21: ronquido, pausas de apnea observadas por los padres, respiración ruidosa, sudoración nocturna, aumento del trabajo respiratorio nocturno, posturas anómalas para dormir con la cabeza hiperextendida, respiración bucal nocturna, enuresis nocturna. De todos ellos, el signo clínico más frecuente en los nińos es el ronquido, siendo éste el motivo inicial de consulta en la mayoría de los casos.
Durante el día nos podemos encontrar con nińos sin ninguna manifestación ni signo clínico, pero también pueden presentar, somnolencia diurna, cansancio, trastornos del comportamiento, hiperactividad, agresividad, alteraciones del crecimiento y retraso escolar.
La somnolencia diurna, síntoma más frecuente en el adulto, no es frecuente en los nińos, clásicamente se ha considerado que fundamentalmente debido a que su estructura de sueńo está más conservada que en el adulto18, sin embargo, este es un tema actualmente en debate, ya que diferentes estudios realizados consideran que la estructura de sueńo no está conservada en los nińos con trastornos respiratorios del sueńo22,23.
MORBILIDAD ASOCIADA AL SAHS EN LOS NIŃOS
DIAGNOSTICO DEL SAHS INFANTIL
La alta prevalencia del SAHS, así como también su importante comorbilidad, ha inducido a la Academia Americana de Pediatría a recomendar que a todos los nińos en los controles de salud habituales, se les realice una historia clínica de sueńo, y si presentan ronquido y además tienen signos o síntomas sugestivos de SAHS, se deben realizar pruebas adicionales7,8.
Los criterios diagnósticos utilizados en el adulto no pueden utilizarse en los nińos. Las técnicas diagnósticas utilizadas en los nińos son:
La PSG nocturna consiste en el registro continuo y supervisado del estado de vigilia y de sueńo espontáneo, mediante el registro de:
Como ya hemos dicho, los criterios diagnósticos del adulto no pueden ser aplicados en los nińos34. Hoy en día sabemos que un Índice de Apneas de 1 es estadísticamente significativo35, pero no sabemos cual es el nivel clínicamente significativo. Posteriormente otros estudios han analizado los valores polisomnográficos normales en nińos y adolescentes, aportándonos datos acerca de estructura de sueńo, arousals y apneas centrales, cuyo significado en nińos ha permanecido incierto durante mucho tiempo36,37, además en un artículo recientemente publicado se encuentran diferencias polisomnográficas en función de la edad de los nińos, estableciéndose dos grupos de edad: menores de 6 ańos y nińos de 6 o más ańos38.
A pesar de todo, la técnica de referencia para el diagnóstico del SAHS en los nińos sigue siendo la PSG nocturna. Los criterios clásicos para el diagnóstico de SAHS son: Presencia de Índice de Apnea Obstructiva (IA) > 1/hora de sueńo, IAH > 5/hora de sueńo, Peak end Tidal CO2 > 53 mmHG, End Tidal CO2 > 50 mmHg durante > 10% del tiempo total de sueńo, SatO2 mínima < 92%39. Más recientemente, se ha propuesto una clasificación de los trastornos respiratorios del sueńo en los nińos, en la cual, no sólo se tienen en cuenta el número de apneas, sino también la saturación de oxigeno, valores de CO2 y número de arousals, clasificándose el SAHS en leve, moderado o grave9.
En base a los conocimientos actuales, "el Grupo de Consenso Espańol de Síndrome de Apneas/Hipopneas durante el sueńo" en el consenso recientemente publicado, acepta un índice de apneas obstructivas entre 1 y 3 como línea de corte de normalidad40.
En el ańo 2002 La American Academy of Pediatrics publica una Normativa para diagnóstico y manejo del Síndrome de Apneas Obstructivas del Sueńo en nińos7,8, realizando una revisión de la literatura de las publicaciones realizadas en nińos entre 2 y 18 ańos desde 1966 al 2000 y concluyen que:
La evaluación clínica41, incluyendo los cuestionarios tiene baja sensibilidad y baja especificidad para el diagnóstico de SAHS en nińos. En cuanto a la utilización de videos domésticos42, concluyen que ha sido inadecuadamente investigado.
La PSG de siesta diurna43 es útil si el resultado es positivo para SAHS, pero un resultado negativo no excluye SAHS y requiere la realización de una PSG nocturna completa. Algo similar ocurre con la Pulsioximetría, en la que incluso un resultado positivo debe ser interpretado con cautela y previa exclusión de enfermedades respiratorias que puedan ocasionar desaturaciones y por tanto dar lugar a falsos positivos. En el estudio realizado por Nixon et al44, se concluye que la Pulsioximetría nocturna puede ser usada para estimar la severidad del SAHS, para reducir el tiempo de diagnóstico y tratamiento en los casos más severos y por tanto, ayudar en la priorización de la adenoamigdalectomia. Este estudio fue realizado en tres fases, las dos primeras de forma retrospectiva supervisando las pulsioximetrias realizadas en nińos que iban a ser sometidos a tratamiento quirúrgico, de los 230 nińos estudiados, 179 (78%) tenían Pulsioximetría normal o no concluyente, los que tuvieron Pulsioximetría positiva para SAHS (22%) no requirieron estudios adicionales y las complicaciones postoperatorias fueron más comunes en los que presentaban mayor alteración en las pulsioximetrias.
La PSG domiciliaria, en el estudio TuCASA45, estudio de cohorte prospectiva, diseńada para valoración de la prevalencia de trastornos respiratorios del sueńo, realizan PSG domiciliaria y concluyen que la PSG multicanal puede ser realizada con éxito en nińos de 5 - 12 ańos de forma no vigilada, pero tan sólo realizan PSG domiciliaria y PSG en laboratorio en 5 de los 157 nińos estudiados.
En cuanto a la Poligrafía Respiratoria (PR), aceptada como alternativa para el diagnóstico de SAHS en el adulto, en el nińo no ha sido adecuadamente validada, aunque la ATS (American Thoracic Society) reconoce que sería una técnica prometedora requiriéndose investigación al respecto. Y otros autores sugieren que el empleo de criterios clínicos junto con una exploración minuciosa de la vía aérea superior, un video domestico y una PR con un equipo validado es una buena alternativa para el diagnóstico de certeza de nińos con sospecha clínica de SAHS19
Hay pocos estudios realizados con PR en nińos, y todos ellos han sido realizados en población de alto riesgo de SAHS, con escaso número de pacientes y sin comparar simultáneamente con la PSG46-48, obteniéndose resultados discordantes.
TRATAMIENTO
El tratamiento de elección del Síndrome de
Apneas/hipopneas durante el sueńo en los nińos es quirúrgico
(adenoamigdalectomia)19,20,21,49:
- 1.- Tratamiento quirúrgico: La eficacia de la
Adenoamigdalectomia, es casi de tres cuartas partes de los casos de
SAHS infantil. Consigue la normalización del cuadro respiratorio
nocturno, de la sintomatología diurna y la reversión en muchos casos
de las complicaciones cardiovasculares, alteraciones neuro-cognitivas
y del retraso en el crecimiento.
El riesgo posquirúrgico pediátrico oscila entre el 0% y el 1,3%,
sin embargo en los nińos con SAHS, se han encontrado tasas de entre el
16-27%50. Se ha reportado mayor incidencia de
complicaciones de la vía respiratoria en estos pacientes, en este
sentido se recomienda monitorización en el postoperatorio de los casos
de más riesgo51: edad menor de 3 ańos, anomalías
craneofaciales, retraso de crecimiento, hipotonía, cor
pulmonale o graves alteraciones en el estudio polisomnográfico
previo a la intervención quirúrgica
Otros tratamientos
quirúrgicos:
Traqueotomía, cirugía plástica maxilar/
mandibular, tratamiento de atresia o estenosis de coanas, revisión del
paladar hendido, uvulopalatofaringoplastia, corrección del tabique
desviado, polipectomía nasal.
Los nińos con SAHS son mayores consumidores de servicios de salud52 y se ha demostrado que el tratamiento del SAHS ocasionado por hipertrofia adenoamigdalar reduce el gasto sanitario en los nińos intervenidos en 1/3. La intervención se asocia a una reducción del 60% de ingresos hospitalarios, el 47% en el número de consultas, reducción en un 39% del número de visitas a servicios de urgencia y una disminución del 27% de gasto farmacológico53.
2.- CPAP nasal:
La CPAP (Presión Positiva Continua
sobre la vía aérea), constituye la segunda línea de tratamiento del
SAHS en la infancia54-58, ya que la mayoría de los nińos
con SAHS se curan con la adenoamigdalectomia, quedando un pequeńo
numero de pacientes que requerirán tratamientos adicionales.
Generalmente suelen ser nińos con obesidad, alteraciones
craneofaciales o enfermedades neuromusculares ańadidas a la
hipertrofia adenoamigdalar o sin hipertrofia adenoamigdalar
Indicaciones de CPAP:
En los casos de tratamiento con CPAP, es necesario controles periódicos puesto que son nińos en crecimiento y desarrollo, siendo necesario vigilancia para evitar el desarrollo de hipoplásias faciales secundarias a uso prolongado, así como vigilancia de los puntos de apoyo. Es necesario, revisión y cambio de mascarillas según velocidad de crecimiento, aproximadamente cada 6 meses.
3.- Oxigenoterapia: Los estudios que han evaluado el efecto del tratamiento con oxigeno en nińos con SAHS59,60
demuestran mejoría de la saturación de oxigeno pero no se observa modificación ni en el número ni en la duración de las apneas obstructivas, en cambio, en algunos individuos se observaba aumento de los niveles de CO2 con el suplemento de oxigeno, por ello no se debe administrar oxigeno a los nińos con SAHS sin una medida previa del cambio de CO2 en respuesta a la administración de oxigeno.
4.- Tratamiento conservador:
Perdida de peso y terapia posicional, es poco efectivo y sólo estaría indicado en nińos mayores con un problema mínimo. Incluso en nińos obesos con hipertrofia adenoamigdalar la primera opción de tratamiento es la adenoamigdalectomia
5.- Tratamiento farmacológico:
En general el
tratamiento farmacológico no es útil en el tratamiento del SAHS.
Últimamente se ha evaluado el papel de los corticoides tópicos en nińos con SAHS leve-Moderado, un estudio evalúa el efecto de 50 mcg de budesonida tópica dos veces al día durante 4 semanas observándose una mejoría clínica que se mantenía hasta 9 meses61. Otro estudio, recientemente publicado evalúa el efecto de los leukotrienos en el tratamiento de nińos con trastornos respiratorios del sueńo leve encontrando una reducción del tamańo adenoideo y del RDI en los nińos tratados con leukotrienos62. Por tanto, estas dos terapias pueden jugar algún papel en el tratamiento de SAHS leves y se requieren más estudios al respecto
6.- Tratamiento profiláctico:
Aunque los
tratamientos ortopédicos no obtienen resultados inmediatos, es
necesario considerar el papel profiláctico que pueda derivarse de un
tratamiento ortodóncico - ortopédico que corrija o mitigue las
anomalías maxilomandibulares en edades tempranas, conduciendo a un
desarrollo adecuado del esqueleto facial.
Podemos concluir esta revisión diciendo que los Trastornos respiratorios del sueńo en edad infantil, en particular el Síndrome de Apneas/Hipopneas durante el sueńo, es una enfermedad frecuente, con presencia de comorbilidad demostrada, que conlleva alteraciones del crecimiento y alteraciones cognitivas en una época de la vida en la que es fundamental el desarrollo físico e intelectual y con un tratamiento efectivo demostrado; Por lo tanto, constituye un problema de salud y todo el personal sanitario estamos obligados a una labor de promoción y prevención de la salud, siendo necesario el diagnóstico y tratamiento adecuado de los nińos con SAHS.
REFERENCIAS
- 1. Osler W: Chronic tonsillitis, in: The principles and
Practice of Medicine. New York, NY, Appleton and co. 1982, pp 335 -
339.
2. Guilleminault C, Eldridge F, Simmons F, et al. Sleep apnea in eight children. Pediatrics 1976; 58: 23 - 30.
3. Gislason T, Benediktsdóttir B. Snoring, apneic episodes, and nocturnal hypoxemia among children 6 months to 6 years old. An epidemiologic study of lower limit of prevalence. Chest 1995; 107: 963 - 966.
4. Blunden S, Lushington K, Lorenzen B, Ooi T, Fung F and Kennedy D. Are sleep problems under- recognised in general practice?. Arch Dis Child 2004; 89: 708 - 712
5. American Thoracic Society. Standards and Indications for Cardiopulmonary Sleep Studies in children. Am J Respir Crit Care Med 1996; 153: 866 - 878
6. American Thoracic Society. Cardiorespiratory Sleep Studies in children. Establishment of normative data and polysomnographic predictors of morbidity. Am J Respir Crit Care Med 1999; 160: 1381 - 1387.
7. American Academy of Pediatrics. Clinical Practice Guideline: Diagnosis and Management of Childhood Obstructive Sleep Apnea Syndrome. Pediatrics 2002; 109 (4): 704 - 712.
8. American Academy of Pediatrics. Technical report: Diagnosis and management of childhood obstructive sleep apnea Syndrome. Pediatrics 2002; 109 (4): e69-e89
9. Katz ES and Marcus CL. Diagnosis of obstructive sleep apnea syndrome in infants and children. En: Sheldon SH, Ferber R, Kryger MH, Editors. Principles and practice of Pediatric sleep medicine. Elsevier Saunders, 2005: p 197 - 210.
10. Ali NJ, Pistón DJ, Stradling RJ. Snoring, sleep disturbance, and behaviour in 4 - 5 years olds. Arch Dis Child 1993; 68: 360 - 366
11. Rosen CL, Storfer-Isser A, Taylor G, Kirchner L, Emancipator J and Redline S. Increased behavioral morbidity in school-aged children with sleep-disordered breathing. Pediatrics 2004; 114; (6)1640-1648.
12. Castronovo V, Zucconi M, Nosetti L, Marazzini C, Hensley M, Veglia F, Nespoli L and Ferini-Strambi L. Prevalence of habitual snoring and sleep-disordered breathing in preschool-aged children in an Italian community. J Pediatr 2003; 142: 377 - 82
13. Redline S, Tishler PV, Schluchter M, Aylor J, Clark K, Graham G. Risk factors for sleep-disordered breathing in children. Associations with obesity, race, and respiratory problems. Am J Respir Crit Care Med 1999; 159: 1527 - 1532
14. Brunetti L, Rana S, Lospalluti ML, Pietrafesa A, Francavilla R, Fanelli M and Armenio L. Prevalence of obstructive sleep apnea syndrome in a cohort of 1.207 children of southern Italy. Chest 2001; 120: 1930 - 1935
15. Sogut A, Altin R, Uzun L, Ugur MB, Tomac N, Acun C, Kart L and Can G. Prevalence of obstructive sleep Apnea Syndrome and associated symptoms in 3-11 year-old Turkish children. Pediatr Pulmonol 2005; 39: 251 - 256
16. Laurikainen E, Aitasalo K, Erkinjuntti M and Wanne O. Sleep apnea syndrome in children secondary to adenotonsillar hypertrophy? Acta Otolaryngol (Stockh) 1992; 492 (Suppl): 38 - 41
17. Marcus Carole l. Sleep disordered Breathing in Children. State of the Art. Am J Respir Crit Care Med 2001; 164: 16 - 30.
18. Marcus CL. Obstructive Sleep Apnea Syndrome: Differences between children and adults. Sleep 2000; 23 (S4): S140 - S141
19. González Pérez-Yarza E, Duran Cantolla J, Sánchez-Armengol A, Alonso Álvarez ML, De Miguel J y Municio JA. SAHS en nińos y adolescentes. Clínica, diagnóstico y tratamiento. Arch Bronconeumol 2002; 38 (supl 3): 34 - 9
20. Messner Anna H and Pelayo Rafael. Pediatric Sleep- Related Breathing Disorders. American Journal of Otolaryngology 2000; 21 (2): 98 - 107
21. Terán Santos J, Alonso Álvarez ML, De Abajo Cucurull C, Cordero Guevara J, González Martínez M, Castrodeza Sanz J. Síndrome d´apnées hypopnées du sommeil chez l´enfant. L´orthodontie francaise 2004; 75 (1): 25 - 29.
22. Tauman R, O´Brien LM, Holbrook CR and Gozal D. Sleep pressure score: A new index of sleep disruption in snoring children. Sleep 2004; 27(2): 274-8
23. O´Brien LM, Tauman R and Gozal D. Sleep pressure correlates of cognitive and behavioral morbidity in snoring children. Sleep 2004; 27(2): 279 - 82
24. Marcus CL, Carroll JL, Koerner CB, et al. Determinants of growth in children with the obstructive sleep apnea syndrome. J Pediatr 1994; 125: 556 - 62.
25. Marcus CL, Greene MG and Carroll JL. Blood pressure in children with obstructive sleep apnea. Am J Respir Crit Care Med 1998; 157: 1098 - 1103
26. Kohyama J, Ohinata JS and Hasegawa T. Blood Pressure in sleep disordered breathing. Arch Dis Child 2003; 88: 139 - 142
27. Amin RS, Carroll JL, Jeffries JL, Grone C et al. Twenty-four-hour ambulatory blood pressure in children with sleep-disordered. Am J Respir Crit Care Med 2004; 169: (8):950 - 956
28. Guilleminault C. Abnormal blood pressure in prepubertal children with sleep-disordered breathing. Pediatr Resp 2004; 55: 76-84
29. Amin RS, Kimball TR, Kalra M, Jeffries JL, Carroll JL, Bean JA, Witt SA, Glascock BJ, Daniels SR. Left ventricular function in children with sleep-disordered breathing. Am J Cardiol 2005; 95: 801 - 804
30. Boudewyns AN and Van de Heyning PH. Obstructive sleep apnea in children: An overview. Acta Otorhino- Laryngologica belga 1995; 49: 275 - 279
31. Guilleminault C, Stoohs R. Chronic snoring and obstructive sleep apnea syndrome in children. Lung 1990; 168 (Suppl): 912 - 919
32. Myatt HM, Beckemham EJ. The use of diagnostic sleep nasendoscopy in the management of children with complex upper airway obstruction. Clin Otolaryngol 2000; 25: 200 - 208
33. Jain A, Sahni JK. Polysomnographic studies in children undergoing adenoidectomy and/or tonsillectomy. The Journal of Laryngol & Otology 2002; 116: 711 - 715
34. Rosen CL, D´Andrea L, Haddad GG. Adult criteria for obstructive Sleep Apnea do not identify chidren with serious obstruction. Am Rev Respir Dis 1992; 146: 1231-1234
35. Marcus CL, Omlin KJ, Basinki DJ et al. Normal polysomnographic values for children and adolescents. Am Rev Respir Dis 1992; 146: 1235 - 1239.
36. Uliel S, Tauman R, Greenfeld M, Sivan Y. Normal polysomnographic respiratory values in children and adolescents. Chest 2004; 125:872-878.
37. Traeger N, Schultz B, Pollock AN, Mason T, Marcus CL and Arens R. Polysomnographic values in children 2 - 9 years old: Additional Data and review of the literature. Pediatr Pulmonol 2005; 40: 22 - 30
38. Montgomery -Downs HE, O´Brien LM, Gulliver TE, Gozal D. Polysomnographic characteristics in normal preschool and early school-aged children. Pediatrics 2006; 117(3): 741-753
39. Carroll JL, Loughin GM. Obstructive sleep apnea Syndrome in infants and children: Diagnosis and management. En: Ferber R, Kryger M, Editors. Principles and practice of sleep in medicine in the child. Philadelphia: WB Saunders, 1995: p 163 - 216.
40. Consenso Nacional sobre el Síndrome de Apneas-Hipopneas del sueńo. Grupo Espańol de Sueńo (GES). El SAHS en la edad pediátrica. Clínica, diagnóstico y tratamiento. Arch Bronconeumol 2005; 41 Supl 4: 81 - 101.
41. Weatherly RA, Ruzicka DL, Marriott DJ and Chervin RD. Polysomnography in children scheduled for adenotonsillectomy. Otolaryngol Head Neck Surg 2004; 131: 727 - 31.
42. Lamm C, Mandeli J and Kattan M. Evaluation of home audiotapes as an abbreviated test for obstructive sleep apnea syndrome (OSAS) in children. Pediatr Pulmonol 1999; 27: 267 - 272.
43. Marcus CL, Keens TG, Ward SL. Comparison of nap and overnight polysomnography in children. Pediatr Pulmonol 1992; 13: 16 - 21
44. Nixon GM, Kermack AS, Davis GM, Manoukian JJ, Brown KA and Broullette RT. Planning adenotonsillectomy in children with obstructive sleep apnea: The role of overnight oximetry. Pediatrics 2004; 113(1): e19-e25
45. Goodwin JL, Enright PL, Kaemingk KL et al. Feasibility of using unattended polysomnography in children for research-report of the Tucson Children's Assessment of Sleep Apnea Study (TuCASA). Sleep 2001; 24 (8) : 937 - 944.
46. Jacob SV, Morielli A, Mograss MA, Ducharme FM, Schloss MD and Brouillette RT. Home testing for pediatric obstructive sleep apnea syndrome secondary to adenotonsillar hypertrophy. Pediatr Pulmonol 1995; 20: 241 - 252
47. Zucconi M, Calori G, Castronovo V and Ferini-Strambi L. Respiratory monitoring by means of an unattended device in children with suspected uncomplicated obstructive sleep apnea. Chest 2003; 124: 602 - 607
48. Poels PJP, Schilder AGM, Van den Berg S, Hoes AW and Joosten KFM. Evaluation of a new device for home cardiorespiratory recording in children. Arch Otolaryngol Head Neck Surg 2003; 129(12): 1281 - 1284
49. Nixon GM, Brouillette RT. Paediatric obstructive sleep apnoea. Thorax 2005; 60: 511 - 516
50. Gutierrez TM. Síndrome de apnea obstructive del sueńo en el nińo: Consideraciones sobre el diagnóstico y el tratamiento quirúrgico. Vigilia-Sueńo 2002; 14: 109 - 116.
51. Rosen GM, Muckle RP, Mahowald MW, Goding GS, Ullevig C. Postoperative respiratory compromise in children with obstructive sleep apnea syndrome: Can it be anticipated?. Pediatrics 1994; 93: 784 - 788
52. Reuveni H, Simon T, Tal A, Elhayany A and Tarasiuk A. Health care services utilization in children with obstructive sleep apnea syndrome. Pediatrics 2002; 110 (1): 68 - 72.
53. Tarasiuk A, Simon T, Tal A, Reuveni H. Adenotonsillectomy in children with Obstructive Sleep Apnea Syndrome Reduces Health Care Utilization. Pediatrics 2004; 113: 351 - 356
54. Massa F, Gonzalez S, Alberti A, Wallis C, Lane R. The use of nasal continuous positive airway pressure to treat obstructive sleep apnea. Arch Dis Child 2002; 87: 438 - 443
55. Waters KA, Everett FM, Bruderer JW, Sullivan CE. Obstructive Sleep Apnea: The use of nasal CPAP in 80 children. Am J Respir Crit Care Med 1995; 152: 780-785
56. Marcus CL, Ward SL, Mallory GB et al. Use of nasal continuous positive airway pressure as treatment of childhood obstructive sleep apnea. J Pediatr 1995; 127: 88 -94
57. McNamara F, Sullivan CE. Obstructive sleep apnea in infants and its management with nasal continuous positive airway pressure. Chest 1999; 116: 10-16
58. Guilleminault C, Pelayo R, Clerk A et al. Home nasal continuous positive airway pressure in infants with sleep-disordered breathing. J Pediatr 1995; 127: 905-912
59. Marcus CL, Carroll JL, Bamford O et al. Supplemental oxygen during sleep in children with sleep-disordered breathing. Am J Respir Crit Care Med 1995; 152(pt 1): 1297-1301
60. Aljadeff G, Gozal D, Bailey-Wahl SL. Effects of overnight supplemental oxygen in obstructive sleep apnea in children. Am J Respir Crit Care Med 1996; 153: 51-55
61. Alexopoulus E, Kaditis A, Kalapouka E, Kostadina E, Angelopoulus N, Mikraki V, Skenteris N, Gourgoulianis N. Nasal corticosterioids for children with snoring. Pediatric Pulmonology 2004; 38: 161-167
62. Goldbart AV, Goldman JL, Veling MC and Gozal D. Leukotriene modified therapy for mild sleep-disordered breathing in children. Am J Respir Crit Care Med 2005; 172: 364-370
Estudios recientes han documentado un método que consiste en la detección de disminuciones de la seńal de fotoplestimográfica del pulso (PPG) basado en la respuesta vasoconstrictora mediada por el sistema nervioso simpático secundario a la hipoxia. La apnea aumenta la actividad simpática., esta se refleja en la disminución de amplitud de las oscilaciones; estas fluctuaciones son detectadas automáticamente y puede servir para cuantificar indirectamente las apneas del sueńo, pero es necesario un estudio con mayor profundidad analizando la relación entre cada evento de disminución de la amplitud y la seńal de las oscilaciones de la PPG.
Esta revisión resulta muy valiosa pues se seńala la necesidad de una labor de promoción y prevención por los profesionales de la salud para asegurar un adecuado diagnóstico y tratamiento precoz de los nińos con trastornos respiratorios durante el sueńo.
Referencias
Comentario del revisor Dra. Marta Sofía López Rodríguez. Especialista en Anestesiología y Reanimación. Profesora Asistente del ISCMH. Facultad Finlay-Albarrán. Clínica Central Cira García Reyes. Habana. Cuba.
Esta revisión aborda ampliamente los desórdenes respiratorios durante el sueńo en los nińos, subrayando la morbilidad seria que producen; menos común ahora, debido al diagnóstico y el tratamiento más temprano. Muchos informes han sugerido que los nińos con desórdenes respiratorios durante el sueńo presentan alteraciones del crecimiento, déficit neurocognitivo, como retraso escolar, problemas de conducta e hiperactividad con déficit de atención. Como en los adultos, el patrón oro para diagnosticar es la polisomnografia; la historia clínica, el examen físico craneo-facial y de la vías aéreas altas han mostrado tener una sensibilidad y especificidad baja para el diagnóstico. Otras pruebas de selección, como la pulsoximetría y la poligrafía respiratoria tienen utilidad limitada como indicativos de desorden de sueńo en nińos. Así, ellos pueden ser útiles inicialmente si polisomnografia no está fácilmente disponible, pero esta última es el instrumento primario para evaluar los desórdenes respiratorios del sueńo. Sin embargo, esto no es una herramienta perfecta.
1. Gil E, López D, Vergara JM, Laguna P. Detección de microdespertares durante el sueńo a partir de la seńal fotopletismográfica. CASEIB 2004:207-10.
2. Schneider H, Schaub CD, Chen CA, Andreoni KA, Schwartz, AR. Neural and local effects of hypoxia on cardiovascular responses to obstructive apnea, J Appl Physiol 2000:1093-1102.
3. Marcus CL. Sleep-disordered Breathing in Children. Am J Respir Crit Care Med 2001;164:16-30.
4. Terán Santos J, Alonso Alvarez ML, Cordero Guevara J, Ayuela Azcárate JM, Monserrat Canal JM, Coma del Corral MJ. Electron J Biomed 2005;1:72-78
