Indice del volumen Volume index
ComitÕ Editorial Editorial Board
ComitÕ CientÚfico Scientific Committee
HëGADO GRASO NO ALCOHÆLICO EN RATAS MACHOS DE UNA LëNEA CON DIABETES GENèTICA
Stella Maris Daniele PhD.1 Juan Carlos Picena PhD.2
Silvana Marisa Montenegro PhD.2,3
MarÚa Cristina TarrÕs PhD. 2,3
Stella Maris MartÚnez PhD.2,3
1Facultad de Ciencias BioquÚmicas
2 Facultad de Ciencias MÕdicas
3 Consejo de Investigaciones. Universidad Nacional de Rosario.
Rosario, Argentina
Rev Electron Biomed / Electron J Biomed 2007;3:29-39
Comentario del revisor Dr. ValentÚn del Villar Sordo. Jefe del Servicio de Medciina Interna del Hospital General de Soria. CatedrÃtico de Medicina de la Universidad de Valladolid. Soria. Espaþa
Comentario del revisor JosÕ Luis HernÃnez CÃceres.Center for Cybernetics Applications to Medicine (CECAM). Havana, Cuba.
ABSTRACT:
Non-alcoholic fatty liver is a common disease closely related to the increasing prevalence of obesity and type 2 diabetes in the general population. The eSS rats display a non obese type 2 diabetic syndrome with an insulin resistant state characterized by hyperglycaemia, hypertriglyceridemia and hyperinsulinemia. In 12 month-old eSS males glycaemia, fructosamine, triglyceridemia and reactive species to oxygen were evaluated, and the hepatic histology was studied. Increased basal glycaemia and fructosamine values correlate directly with those of lipid peroxidation and inversely with antioxidant values. Diffuse steatosis was detected. Cytoplasmatic PAS positive granularity decreased towards the center of the lobule. Binucleated hepatocytes were observed, as well as regular mobilization of Kupffer cells. The pattern of lipidic deposits in eSS rat's hepatocytes was similar to the one observed in biopsies of type 2 diabetic patients. As eSS displays a diabetic syndrome without obesity, these findings suggest the capacity of increased levels of oxidative stress to induce hepatic steatosis.
Key words: Rats, biologic models, hepatic steatosis, diabetes, oxidative stress
RESUMEN:
El hÚgado graso no alcohµlico (HGNA) es una entidad de prevalencia creciente en todo el mundo vinculada a la obesidad y a la diabetes tipo 2. Las ratas eSS presentan un sÚndrome diabÕtico tipo 2 espontÃneo, sin obesidad, con un estado de resistencia a la insulina caracterizado por hiperglucemia, hipertrigliceridemia e hiperinsulinemia. En machos eSS de 12 meses fueron evaluadas glucemia, fructosamina (FH2), trigliceridemia y especies reactivas al oxÚgeno, asÚ como la histologÚa hepÃtica. Se verificµ aumento de la glucemia basal y de la FH2 cuyos valores correlacionan directamente con los de los indicadores de peroxidaciµn lipÚdica e inversamente con antioxidantes totales. Se observµ esteatosis y granularidad citoplasmÃtica PAS positiva en los hepatocitos. Asimismo, se detectaron imÃgenes de binucleaciµn hepatocelular y regular movilizaciµn de cÕlulas de Kupffer. El patrµn de los depµsitos lipÚdicos y de la granularidad citoplasmÃtica en los hepatocitos es anÃlogo al observado en biopsias de pacientes diabÕticos tipo 2. De esta manera, eSS presenta un sÚndrome diabÕtico sin obesidad lo cual sugiere la capacidad del estrÕs oxidativo resultante de inducir esteatosis hepÃtica.
Palabras clave: ratas, modelos biolµgicos, esteatosis hepÃtica, diabetes, estrÕs oxidativo
INTRODUCCIÆN
El hÚgado graso no alcohµlico (HGNA) incluye un amplio espectro de lesiones hepÃticas que van desde la esteatosis, pasando por la esteatohepatitis hasta la fibrosis y, eventualmente, la cirrosis1.
La esteatosis hepÃtica no alcohµlica, caracterizada por la acumulaciµn de lÚpidos visibles en el citoplasma de los hepatocitos de pacientes sin antecedentes de consumo de alcohol, fue considerada largo tiempo una entidad de curso benigno2. Actualmente se admite que la esteatosis aumenta la vulnerabilidad del hepatocito frente a otras agresiones3, pudiendo ser el primer paso de un proceso de daþo hepÃtico en que se agreguen lesiones inflamatorias de mayor gravedad4.
La obesidad, la diabetes tipo 2 y la hiperlipemia son causas primarias del HGNA5. Se estima que el 75% de los pacientes diabÕticos tipo 2 presenta en mayor o menor grado alguna de las etapas de HGNA. Su etiopatogenia està vinculada con la resistencia a la insulina, el estrÕs oxidativo asÚ como a factores genÕticos y ambientales no bien conocidos6. Se lo ha vinculado a procesos adaptativos de supervivencia de poblaciones humanas y animales en ambientes muy frÚos y con escasa disponibilidad alimenticia7.
Las ratas eSS desarrollan espontÃneamente una diabetes tipo 2, sin obesidad, mÃs marcada en los machos. Hasta el aþo se produce el aumento de la glucemia junto a niveles crecientes de insulina circulante lo que indica resistencia a la insulina8-9. Durante el segundo aþo, se comprueba la disminuciµn progresiva de las concentraciones de insulina y el agravamiento del sÚndrome8-9. Las alteraciones del metabolismo lÚpido son precoces y se ha comprobado niveles aumentados de triglicÕridos plasmÃticos en machos de 5 meses de edad, aun euglicÕmicos10.
El presente estudio demuestra la presencia de lesiones caracterÚsticas del HGNA en machos eSS de un aþo de edad, atribuibles a su dismetabolopatÚa y al consecuente estrÕs oxidativo.
MATERIAL Y MèTODOS
Se utilizaron machos eSS y controles Wistar (W) eumetabµlicos de 12 meses de edad. Los machos eSS provenÚan del bioterio de la CÃtedra de BiologÚa de la Facultad de Ciencias MÕdicas de la UNR. Los machos W pertenecÚan al bioterio de la Facultad de Ciencias BioquÚmicas-UNR. Las condiciones de crÚa incluyen regulaciµn de la temperatura (24¤C) y de los ciclos luz-oscuridad asÚ como el recambio de aire. En todos los casos los individuos permanecieron alojados desde los 21 dÚas de edad, en jaulas colectivas suspendidas y sin lecho. Los animales recibieron agua y alimento balanceado ad libitum. Este ºltimo en forma de pellets secos (Cargill rata-ratµnR, Cargill Co., Buenos Aires) que cada 100 g contienen: proteÚnas 25.1%, grasa 3.5%, glºcidos (almidµn) 43%, fibra 6%, minerales 8%, vitaminas 1.9% y humedad 12.5%. La densidad calµrica fue de 304 Kcal/100 g.
El protocolo de investigaciµn fue examinado y considerado aceptable desde el punto de vista Õtico por la Comisiµn de BioÕtica de la Facultad de Ciencias MÕdicas-UNR.
1. ExÃmenes de laboratorio:
Se emplearon 12 machos eSS y 10 W para la determinaron la glucemia basal (G0), la fructosamina (FH2) y los triglicÕridos plasmÃticos (Tg). Asimismo, se determinaron las especies µxido reactivas con Ãcido tiobarbitºrico (TBARS) que es un marcador de la peroxidaciµn lipÚdica basado en la reacciµn del malondialdehido (MDA) con el Ãcido tiobarbitºrico (TBA). Los factores implicados en la protecciµn antioxidante fueron evaluados mediante la determinaciµn del estado de los antioxidantes totales (TAS), el Ãcido ºrico (Ur) y la superµxido dismutasa (SOD).
DespuÕs de un ayuno de 10 horas, se pesµ a los animales, se los anestesiµ y se obtuvieron las muestras de sangre por punciµn cardÚaca. Las muestras fueron divididas en dos fracciones, una de las cuales recogida sobre EDTA (1mg/ml) y dividida a su vez en dos porciones. Una de las alÚcuotas fue centrifugada durante 10 minutos a 1500 G, separado el plasma del paquete globular y conservado a -20 ¤C hasta la determinaciµn de TBARS dentro de las 72 h, mientras que la otra porciµn fue destinada a determinar SOD y el contenido de hemoglobina, determinaciones realizadas despuÕs de la extracciµn. La segunda fracciµn de sangre entera fue centrifugada durante 10 minutos a 1500 g, luego fue separado el suero y en una parte de Õste se cuantificaron glucemia y FH2, mientras que otra porciµn se conservµ a -20 ¤C hasta la determinaciµn de TAS, dentro de los 14 dÚas siguientes.
Previa determinaciµn del contenido de hemoglobina, se midiµ la SOD utilizando el Kit Ransod de los laboratorios Randox Ltd. (Cat. N¤ SD125). Se centrifugaron alÚcuotas de sangre, se lisaron los hematÚes. El lisado se utilizµ para la medida de la SOD.
En la determinaciµn de TBARS, el procedimiento analÚtico empleado fue adaptado de los mÕtodos desarrollados por Hendriks y Assman11 y por Richard y col.12. 50 ml de plasma (o la soluciµn standard de trabajo de MDA) se colocaron en un tubo de vidrio de 10 ml conteniendo 1 ml de agua destilada a los que se les adicionµ 1ml de soluciµn conteniendo 29 çmol/L de TBA, en Ãcido acÕtico (pH entre 2.4 a 2.6). Las muestras fueron colocadas en un baþo de agua durante 1 h a 95-100 ¤C. El producto coloreado fue extraÚdo por agitaciµn con n-butanol. Se separµ la capa de n-butanol por centrifugaciµn a 1500 G durante 10 minutos y se midiµ la absorbancia a 532 nm). Se analizµ el TAS utilizando un Kit de Laboratorios Randox Ltd. (Cat. N¤ NX2332). Respecto de eSS, se completµ el procedimiento en 8 muestras.
Para la determinaciµn de FH2, se midiµ la absorbancia en la reacciµn reducciµn del azul de nitrotetrazolium. Los niveles de glucosa sÕrica y de triglicÕridos se determinaron en autoanalizador Hitachi 912.
En eSS, fueron calculadas las correlaciones entre TBARS y G0; TBARS y FH2; TAS y G0; TAS y FH2; TBARS y TAS y entre TAS y SOD. Asimismo, se estimµ la correlaciµn entre Tg y TAS, TBARS y SOD, respectivamente.
2. Estudio anatomopatolµgico:
En 6 machos eSS y 6 W, se registrµ la biomasa, se los sacrificµ e inmediatamente se extrajo el hÚgado y se lo pesµ. Parte del µrgano fue fijado en parafina para realizar cortes histolµgicos y teþirlos con H-E y PAS. Otra parte fue sometida a la tÕcnica de cortes por congelaciµn y tinciµn especial (Oil Red o Rojo O) para visualizar lÚpidos. Posteriormente se realizµ el estudio con microscopÚa µptica.
3. MÕtodos estadÚsticos:
Los resultados se expresan como media Ý ES y se analizaron mediante la prueba t de Student. Las correlaciones bivariadas entre TBARS, G0, FH2, TAS y SOD se calcularon mediante el coeficiente r de Pearson. Se asumiµ un nivel de significaciµn de p<0.05.
Los animales fueron tratados respetando las normas Õticas que rigen el empleo de animales de investigaciµn.
RESULTADOS
G0, FH2 y Tg fueron significativamente superiores en eSS mientras que los valores de la biomasa no difirieron. En las ratas diabÕticas se verificaron niveles mÃs altos del marcador de lipoperoxidaciµn TBARS y una disminuciµn significativa del estado de los antioxidantes totales TAS respecto de los animales controles. En cuanto a la actividad SOD y la concentraciµn de Ur, no hubo diferencias significativas entre lÚneas (Tabla1).
|
Línea |
Peso (g) |
G0 (mg/dl) |
Tg (mg/dl) |
FH 2 |
TBARS (umol/l) |
TAS (mmol/l) |
Ur (mg/dl) |
SOD U/g Hb |
|
eSS (n=12) |
424 Ý 11 |
148 Ý 7.7 |
167 Ý 7.4 |
193 Ý 16.4 |
11 Ý 1.8 |
0.48* Ý 0.027 |
1.38 Ý 0.5 |
2060 Ý 100 |
|
Wistar (n=10) |
413 Ý 33 |
99 Ý 7.3 |
53 Ý 4.1 |
101 Ý 18.7 |
3.4 Ý 0.62 |
0.88 Ý 0.047 |
1.22 Ý 0.4 |
2111 Ý 83 |
|
P |
>0.05 |
<0.001 |
<0.001 |
<0.001 |
<0.001 |
<0.001 |
>0.05 |
>0.05 |
Los valores se expresan como media ± ES *: Los valores corresponden a 8 animales
Se verificaron correlaciones significativas entre los niveles de TBARS y G0 (r: 0.909), asÚ como entre TBARS y FH2 (r: 0.911). TambiÕn se comprobaron correlaciones negativas y significativas entre G0 y TAS (r: -0.9), FH2 y TAS (r: -0.921) y TBARS y TAS (r: -0.943) (Figuras 1, 2, 3, 4 y 5). No hubo correlaciones significativas entre TBARS y TAS ni entre TBARS y SOD. Tampoco se verificµ correlaciµn entre Tg con ninguna de las variables consideradas.
En los animales autopsiados se comprobµ que el peso del hÚgado fue superior en eSS respecto de W (eSS: 25.07±5.63 g vs. 16.42±1.28 g; P < 0.001) pese a tener biomasas similares (eSS: 420±6.33 g vs. W: 435±38 g; p>0.05).
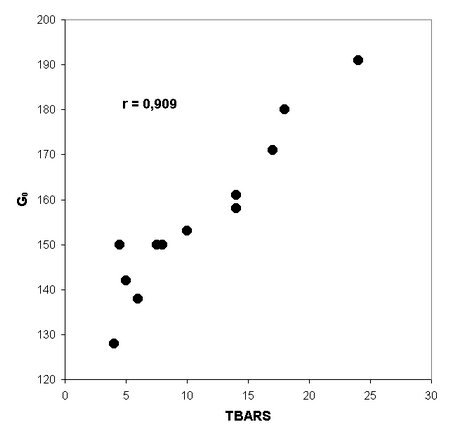
Fig. 1: Correlaciµn entre los valores de sustancias Ãcido reactivas con Ãcido tiobarbitºrico en suero (TBARS) medidos en çmol/L, y los de la glucemia basal (G0) dosada en mg/dl, en 12 ratas machos diabÕticas de lÚnea eSS, de 12 meses de edad (r = 0.909; p<0.001).
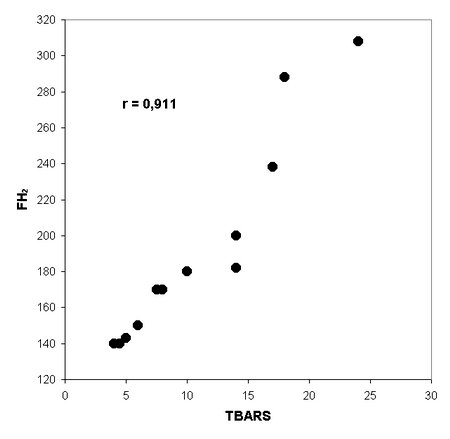
Fig. 2: Correlaciµn entre los valores de sustancias Ãcido reactivas con Ãcido tiobarbitºrico en suero (TBARS) medidos en çmol/L, y los de la fructosamina glucosilada (FH2) en 12 ratas machos diabÕticas de lÚnea eSS, de 12 meses de edad (r=0.911; p<0.001).
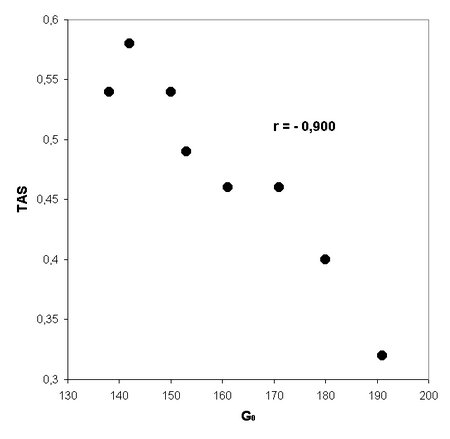
Fig. 3: Correlaciµn entre los valores de la fructosamina (FH2) y los de antioxidantes totales (TAS) medido en çmol/L en 8 ratas machos diabÕticas de lÚnea eSS, de 12 meses de edad (r=-0.900; p<0.01).
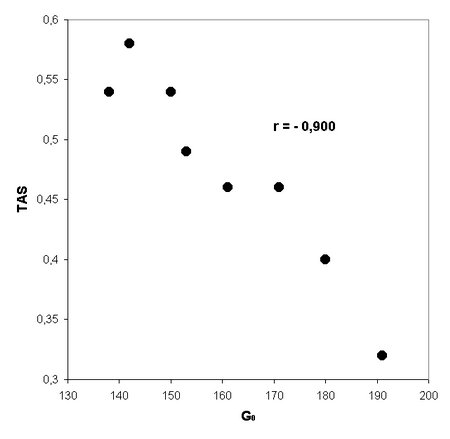
Fig. 4: Correlaciµn entre los valores de la glucemia basal (G0) dosada en mg/dl, y los de antioxidantes totales (TAS) medido en çmol/L en 8 ratas machos diabÕticas de lÚnea eSS, de 12 meses (r=-0.900; p<0.01).

Fig. 5: Correlaciµn entre los valores de la fructosamina (FH2) y los de antioxidantes totales (TAS) medido en umol/L çmol/L en 8 ratas machos diabÕticas de lÚnea eSS, de 12 meses de edad (r=-0.921; p<0.01).
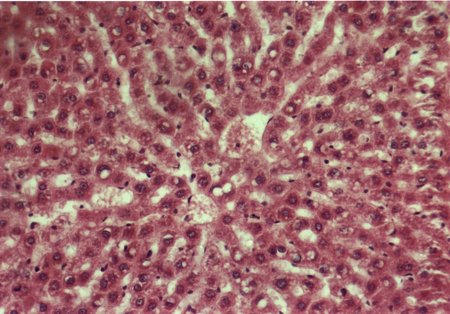
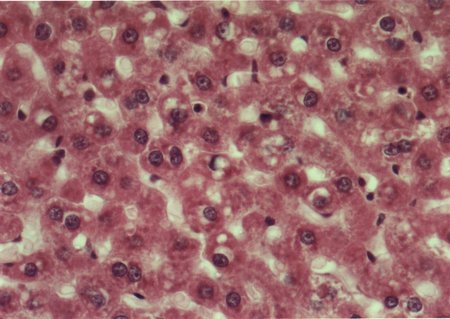
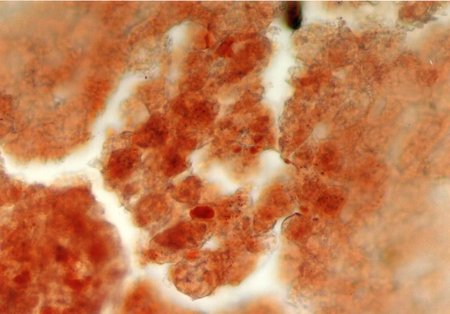
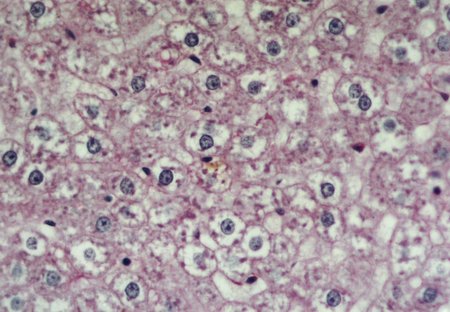
Al estudiar la histologÚa hepÃtica, se observµ que en eSS las estructuras lobulillar, trabecular y portal no presentaron alteraciones. Los animales diabÕticos exhibieron esteatosis caracterizada por vacuolas de distintos tamaþos mÃs abundantes en la zona centro y mediolobulillar (figs 6 y 7), que se colorean con Oil Red (fig 8), asÚ como granularidad citoplasmÃtica de los hepatocitos (fig 9). Se observa la presencia de balonizaciµn, binucleaciµn hepatocelular, asÚ como incremento de las cÕlulas de Kupffer (fig 10). Con la tinciµn de PAS se aprecia una positividad difusa, caracterÚstica de los depµsitos de glucµgeno, que disminuyen hacia el centro del lobulillo (fig 9). En algunas zonas existÚan focos de colestasis (fig 11). No se detectµ signos de inflamaciµn lobulillar ni portal, ni de fibrosis.
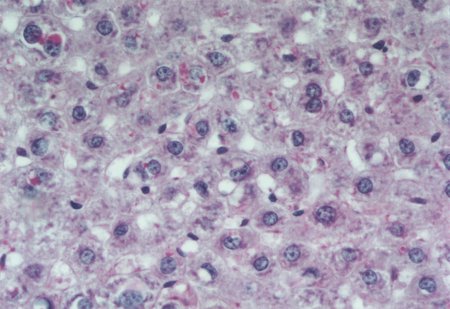
Fig. 9: Granularidad y vacuolizaciµn del
citoplasma hepatocelular. Depµsitos PAS positivos. PAS-400X
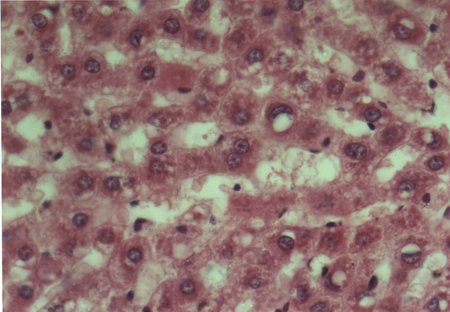
Fig. 10: Vacuolas de distintos tamaþos y balonizaciµn.
Hepatocito binucleado en el centro. CÕlulas de Kupffer prominentes. HE-400X
En los testigos Wistar la estructura de los lobulillos, la disposiciµn de las trabÕculas, la conformaciµn de los espacios portales y las caracterÚsticas citoplasmÃticas no presentaron alteraciones.
DISCUSIÆN
La presencia de esteatosis y balonamiento hepatocelular, asÚ como la movilizaciµn de cÕlulas de Kupffer en el hÚgado de las ratas eSS, sugiere un hÚgado graso no alcohµlico. Cabe mencionar que la Asociaciµn Americana para el Estudio de las Enfermedades del HÚgado definiµ como criterios para el diagnµstico de la EHNA en humanos la presencia de esteatosis en combinaciµn con hepatocitos balonizados, asÚ como de infiltrado inflamatorio mixto acompaþado, en ocasiones, de fibrosis13. Como este ºltimo criterio no se observµ en los animales eSS, se estarÚa ante la etapa inicial de su esteatohepatitis.
El primer paso de la enfermedad hepÃtica no alcohµlica, la esteatosis aparentemente es causada por la resistencia perifÕrica a la insulina que incrementa el transporte de Ãcidos grasos al hÚgado y la sÚntesis intrahepÃtica de triglicÕridos14. A su vez, esto promueve mayor acumulaciµn de triglicÕridos a travÕs de la inhibiciµn de la oxidaciµn mitocondrial de los Ãcidos grasos15. Tales fenµmenos intervendrÚan en la apariciµn de esteatosis en la rata eSS, ya que la lÚnea diabÕtica presenta niveles crecientes de insulina circulante hasta el aþo edad junto a glucemias cada vez mÃs elevadas lo que indica resistencia a la insulina8-9.
Es interesante seþalar que eSS no presenta obesidad, uno de los factores de riesgo claramente asociados al HGNA. Sin embargo, si bien la esteatosis està presente en el 70% de los pacientes diabÕticos obesos, tambiÕn lo està en el 35% de los pacientes con peso normal14. El hÚgado graso no parece ser un rasgo uniforme del sÚndrome metabµlico y parecerÚa existir una gran variaciµn individual en su desarrollo7.
En eSS la hiperglucemia se asocia con altos niveles de lipoperoxidaciµn asÚ como la disminuciµn de las defensas antioxidantes. Los valores elevados de FH2 indican que la hiperglucemia es sostenida en el tiempo y, por lo tanto, capaz de inducir productos finales de glicosilaciµn avanzada. Se sabe que los mismos estÃn involucrados en la generaciµn de especies reactivas derivadas del oxÚgeno altamente tµxicas para las cÕlulas15. El desequilibrio glucÕmico crµnico de eSS inducirÚa el incremento de radicales libres capaces de atacar los dobles enlaces de los Ãcidos grasos poliinsaturados, induciendo lipoperoxidaciµn y un mayor daþo celular oxidativo. Estos resultados coinciden con los hallazgos en la diabetes humana tipo 216. De este modo, si bien la resistencia a la insulina serÚa el factor clave en el inicio de la acumulaciµn grasa en el hÚgado, una vez que la esteatosis se establece, el estrÕs oxidativo es un factor fundamental que promueve mayor daþo hepatocelular y la evoluciµn de las lesiones14, 17-18.
La movilizaciµn de cÕlulas de Kupffer observada en eSS indicarÚa la existencia de un proceso inflamatorio hepatocelular. Se sabe que su activaciµn conduce a la liberaciµn de citoquinas pro-inflamatorias, tales como el factor de necrosis tumoral alfa, vinculadas a la evoluciµn de la esteatosis a la esteatohepatitis14, 19-20. Asimismo, como el hallazgo de binucleaciµn hepatocelular es un indicio de regeneraciµn, parecerÚan coexistir en forma simultÃnea lesiones alterativas celulares e intentos compensatorios que se oponen a ellas.
En conclusiµn, los machos de la lÚnea diabÕtica eSS presentan al aþo lesiones hepÃticas propias del hÚgado graso no alcohµlico. La resistencia a la insulina como fenµmeno inicial y su combinaciµn con el estrÕs oxidativo debido a la persistencia de elevadas glucemias, serÚan factores determinantes de su patogÕnesis. No se descarta la existencia de lesiones hepÃticas en machos eSS mÃs jµvenes ya que se sabe que la resistencia a la insulina està presente desde los primeros meses de vida8-9.
REFERENCIAS
1. Adams LA, Angulo P, Lindor KD. Non-alcoholic fatty liver disease. CMAJ 2005; 172: 899-05.
2. Teli MR, James O, Burt A, Bennett MK, Day CP. The natural history of nonalcoholic fatty liver: a follow-up study. Hepatology 1995; 22:1714-19
3. Day CP. Pathogenesis of steatohepatitis. Best Pract Res Clinical Gastroenterol 2002; 16: 663-78.
4. Farell GC. Non alcoholic steatohepatitis: What is it, and why is it important in the Asian-Pacific region? J Gastroenterol Hepatol 2003; 18: 124-38.
5. Adams LA, Angulo P. Treatment of non-alcoholic fatty liver disease. Postgrad Med J 2006; 82: 315-22.
6. Hoque M, Sanyal AL. The metabolic abnormalities associated with non-alcoholic fatty liver disease. Best Pract Res Clin Gastroenterol 2002; 16: 709-31.
7. Caldwell SH, Ikura Y, Iezzoni JC, Liu Z. Has natural selection in human populations produced two types of metabolic syndrome (with and without fatty liver)? J Gastroenterol Hepatol 2007; 22 (Suppl 1):S11-9.
8. MartÚnez SM, TarrÕs MC, Montenegro SM, Revelant G, Figueroa N, Alonso D, Laudanno OM, DÇOttavio A. Intermittent dietary restriction in eSS diabetic rats. Effects on metabolic control and skin morphology. Acta diabetol lat 1990; 27: 329-36.
9. MartÚnez SM, TarrÕs MC, Picena JC, Montenegro SM, Gagliardino JJ, Gµmez-Dumm, CLA, D'Ottavio AE, Naves A, Rabasa SL. eSS rat, an animal model for the study of spontaneous non-insulin-dependent diabetes. In: Lessons from animal diabetes IV; E Shafrir ed. Smith Gordon, London 1993, pp 75-90.
10. Gomez Dumm INT., Montenegro S, Tarres MC, Martinez SM, Igal RA. Early Lipid Alterations in Spontaneously Diabetic Rats. Acta Physiol Pharmacol Ther Latinoam 1998; 48: 228-34.
11. Hendriks T, Assmann RFTA. On the fluorometric assay of circulating lipoperoxides. Clin Chem Acta 1988; 174: 263-70.
12. Richard MJ, Portal B, Meo J, Coudray C, Hadjian A, Favier A. Malondialdrhyde kit evaluated for determining plasma and lipoprotein fractions that react with thiobarbituric acid. Clin Chem 1992; 38: 704-9.
13. Neuschwander-Tetri BA, Caldwell S. Nonalcoholic steatohepatitis: summary of an AASLD single Tepic Conference. Hepatol 2003, 37: 1202-19.
14. Medina J, Fernandez-Salazar LI, Garcia-Buey L, Moreno-Otero R. Approach to the pathogenesis and treatment of nonalcoholic steatohepatitis. Diab Care 2004; 27:2057-66.
15. Browning JD, Horton JD. Molecular mediators of hepatis steatosis and liver injury. J Clin Invest 2004; 114: 147-152.
16. Aguirre F, Martin I, Grinspon D, Ruiz M, Hager A, De Paoli T, Ihlo J, Farach HA, Poole CP. Oxidative damage, plasma antioxidant capacity, and glucemic control in elderly NIDDM patients. Free Radic Biol Med 1998; 24:580-85.
17. G—kkusu C, Palanduz S, Ademoglu E, Tamer S. Oxidant and antioxidant systems in NIDDM patients: influence of vitamin E supplementation. Endocr Res 2001; 27:377-86.
18. Leclercq IA. Pathogenesis of steatohepatitis: insights from the study of animal models. Acta Gastroenterol Belg 2007; 70:25-31.
19. Wigg AJ, Roberts-Thomsom IC, Dymock RB, McCarthy PJ, Grose RH, Cummins AG. The role of intestinal bacterial overgrowth, intestinal permeability, endotoxemia, and tumor necrosis factor alfa in the pathogenesis of non-alcoholic steatohepatitis. Gut 2001; 48: 206-211.
20. Leclercq IA, Da Silva Morais A, Schroyen B, Van Hul N, Geerts A. Insulin resistance in hepatocytes and sinusoidal liver cells: mechanisms and consequences. J Hepatol 2007; 47: 142-56.
Correspondencia:
Prof Dra Stella Maris MartÚnez
Facultad de Ciencias MÕdicas- UNR
Santa Fe 3100
2000 Rosario, Argentina
Correo electrµnico: stellamartinez @ telnet.com.ar
Recibido 17 de Octubre de 2007. Recibido revisado 27 de Diciembre.
Publicado 31 de Diciembre de 2007