Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
- Caso nuevo. Paciente sin antecedentes de tuberculosis ni de tratamiento antituberculoso previo.
- Fracaso de tratamiento. No observar conversión bacteriológica después de tres meses de tratamiento.
- Recaída. Hallazgo de un frotis positivo (BAAR) y/o aislamiento de M tuberculosis en un paciente que completa los 6 meses de tratamiento.
- Cura probable. Paciente en el que, una vez finalizados los 6 meses de tratamiento, no sufre ni recaída ni fracaso de tratamiento.
- Cura. Paciente en el que, una vez finalizado su tratamiento, no se observa ninguna recaída después de 12 meses de seguimiento posterior.
EFECTO TERAPÉUTICO DE QUINOLONAS EN 29 PACIENTES CON TUBERCULOSIS GENITOURINARIA: 18 AÑOS DE SEGUIMIENTO
Armando Alberte Castiñeiras1 Pilar Pérez Pascual1,Cristina Alberte Pérez2, José M Martinez-Sagarra Oceja3
1Microbiología y 3 Urología. Hospital del Río Hortega, Valladolid. 2Gerencia de Atención Primaria.
Segovia. España.
aalberte @ hurh.sacyl.es
Rev Electron Biomed / Electron J Biomed 2008;1 9-19
Comentario del revisor Prof. Francisco Abad Santos, MD. PhD. Farmacología Clínica. Hospital la Princesa y Universidad Autónoma de Madrid. España.
Comentario del revisor Prof. José María Eirós Bouza MD. PhD. Titular de Microbiología de la Universidad de Valladolid. España
RESUMEN
INTRODUCCIÓN. Valorar la eficacia bacteriológica de un tratamiento con quinolonas en tuberculosis genitourinaria, en un seguimiento de más de diez años.
MATERIAL Y MÉTODOS. Veinte y nueve pacientes con TBU, casos nuevos, fueron tratados con ofloxacino (200 mg cada 12 h. vo., 6 meses), rifampicina (600 mg/día vo., 3 meses) e isoniacida (300 mg/día vo., 3 meses), entre 1989 y 1992, diagnosticados por aislamiento de M tuberculosis de las orinas procesadas. Se asumió la conversión bacteriológica (negativización) como un signo clínico de eficacia, comparándola, como única variable, con un grupo control de 150 enfermos con tuberculosis genitourinaria que recibieron tratamiento convencional. El seguimiento fue realizado, en ambos grupos, mensualmente durante los seis primeros meses, seis meses más tarde y, posteriormente a lo largo de diez años después de la finalización del tratamiento.
RESULTADOS. El cultivo fue positivo con más de 100 colonias en el 62% de los pacientes, siendo el frotis positivo en el 56%. Todas las cepas de M tuberculosis fueron sensibles a rifampicina, isoniacida y ofloxacino. Tres pacientes abandonaron el tratamiento. La conversión bacteriológica (negativización) fue (en porcentajes) del 92.6 (primero y segundo mes) y 100 en los siguientes estudios. En el grupo control, con terapia tradicional, la conversión fue: 90, 87, 93 y 100 en los restantes. El tratamiento con ofloxacino mostró una conversión bacteriológica similar al tratamiento convencional (p>0.05, test exacto de Fisher).
CONCLUSIÓN. Ofloxacino, en combinación con rifampicina e isoniacida, mostró una respuesta bacteriológica y clínica eficaz, en la tuberculosis genitourinaria.
PALABRAS CLAVE: Tratamiento de la tuberculosis; Tuberculosis urinaria; Ofloxacino; Conversión bacteriológica, quinolonas.
SUMMARY
BACKGROUND. The aim of this study was to evaluate the antibiotic therapy efficacy of quinolones in genitourinary tuberculosis.
MATERIAL AND METHODS. Twenty nine patients with urinary tuberculosis were treated with ofloxacin (200 mg/12 h, 6 months), rifampin (600 mg/day, 3 months) and isoniazid (300 mg/day, 3 months) between 1989 and 1992. All patients, new cases, were diagnosed by isolation of Mycobacterium tuberculosis in one of the three morning urine samples. Bacteriological culture conversion (negativization) was assesed as a clinical guide of efficacy, comparing it, as the only parameter, against a control group (150 patients) with genitourinary tuberculosis and conventional therapy. Bacteriological follow-up studies were performed in both groups monthly for 6 months, then again 6 months later and then every year for 10 years after completion of treatment.
RESULTS. In the 29 patients, the initial culture was positive with over 100 colonies per culture (62%), and the smear was positive in 56% of the patients. All strains were susceptible to rifampicin, isoniazid and ofloxacin. Three patients discontinued therapy, one due to liver disease and another due to an allergic reaction and the third for not compliance. Beginning with the first month of treatment, the bacteriological conversion was 92.6% (first and second month) and 100% in the remaining controls. In the control group, wich received conventional treatment, the conversion was: 90%, 87%, 93% and 100% in the remaining controls. Treatment with ofloxacin showed a bacteriological conversion similar to the conventional treatment (p>0.05, Fisher`s exact test).
CONCLUSION. After 10 years of patient follow-up, we conclude that ofloxacin, in combination with rifampin and isoniazid (both for 3 monts only) is effective in genitourinary tuberculosis, providing satisfactory bacteriological and clinical efficacy.
KEY WORDS: Tuberculosis therapy; Urinary tuberculosis; Ofloxacino; Tuberculosis conversion, quinolones.
INTRODUCCION
La tuberculosis (TB), enfermedad causada por Mycobacterium tuberculosis, puede ser mortal si no se la trata adecuadamente. La incidencia de tuberculosis está aumentando aproximadamente un 0.4% por año, observándose este incremento principalmente en el Africa subsahariana y en los diferentes países de la antigua Unión Soviética (WHO 2003a). En cuanto a la morbi-mortalidad, cada año contraen la enfermedad unos ocho millones de personas, muriendo aproximadamente dos millones1.
En todas sus formas de presentación clínica, la tuberculosis continúa teniendo una incidencia alta en nuestro medio2. Actualmente, las pautas de tratamiento, que están bien definidas3-5, tienen una duración de 6 meses (pauta corta) o de 9 meses. En la pauta corta se adiciona, piracinamida a la combinación de rifampicina (RMP) e isoniacida (INH). Aunque la eficacia de este tratamiento ha sido demostrada plenamente, su uso puede originar efectos secundarios indeseables. De ahí la búsqueda constante de nuevas posibilidades terapéuticas7, cuyos objetivos pretenden reducir la duración del mismo, sin perder la eficacia, disminuyendo los efectos secundarios de los fármacos utilizados, propiciando la adhesión al mismo por parte del paciente8.
La aparición de las quinolonas fluoradas, con actividad frente a M tuberculosis, las hace interesantes en el tratamiento de la TB, por disponer de una farmacocinética favorable y de una baja toxicidad9-12. Ofloxacino presenta una buena biodisponibilidad consiguiendo concentraciones sanguíneas altas, siendo la eliminación renal superior al 90% durante las primeras 24 horas después de su administración13. Por otra parte, también ha demostrado su eficacia en el tratamiento de la tuberculosis primaria, tanto en monoterapia como asociado a otros fármacos antituberculosos14, con los cuales no presenta ni antagonismos ni reacciones cruzadas15-16. En general, las fluoroquinolonas pueden aportar los siguientes beneficios en los regímenes antituberculosos: por un lado, incrementan el efecto bactericida y esterilizador del tratamiento combinado al inhibir la girasa-ADN, aumentando la penetración en los focos de la infección, y, en segundo lugar, mejoran el cumplimiento del tratamiento, debido al perfil de seguridad que presentan17.
Por todo ello, consideramos oportuno, en 1989, investigar la eficacia de ofloxacino, asociado a otros fármacos antituberculosos (isoniacida y rifampicina), en el tratamiento de la TB genitourinaria. Como marcador de la eficacia del tratamiento se consideró la conversión bacteriológica (negativización) de las muestras urinarias estudiadas, así como el seguimiento realizado en casi dos décadas a los 29 pacientes incluidos dentro del estudio con objeto de detectar recaídas o fracasos del mismo. Este estudio se comparó con un grupo control de 150 pacientes tratados con la pauta corta de seis meses. Finalmente, se valora la novedad que representó, en aquel momento, dicho régimen terapéutico en nuestro País.
MATERIAL Y MÉTODOS
Pacientes: criterios de inclusión
a. Pacientes tratados con ofloxacino
Fueron incluidos 29 pacientes (14 mujeres y 15 hombres), con edades comprendidas entre 16 y 67 años (media de 50.7 años) con tuberculosis genitourinaria confirmada bacteriológicamente. Se excluyeron embarazadas, madres en periodo de lactancia y menores de 15 años (Tabla 1). Todos eran casos nuevos, es decir, pacientes que no habían sido diagnosticados ni tratados previamente de tuberculosis. Todos los pacientes fueron informados según las normas establecidas, dando su consentimiento. La tuberculosis genitourinaria fue diagnosticada por aislamiento de M tuberculosis de una de las tres muestras de orina matutina remitidas al laboratorio.

b. Grupo control
Constituido por 150 pacientes diagnosticados microbiológicamente de tuberculosis genitourinaria en los cinco años anteriores, a los cuales se les había realizado el mismo protocolo de seguimiento bacteriológico que el grupo de estudio, con objeto de comparar la eficacia de ambas pautas en términos de conversión bacteriológica.
Definiciones
Investigación y controles microbiológicos
Las muestras fueron procesadas siguiendo la técnica de decontaminación con ácido sulfúrico al 6%18, procediéndose, a partir del sedimento obtenido, a realizar el frotis para visualización y el cultivo en medio de Lowenstein Jensen y piruvato, incubándose a 35ºC durante un periodo máximo de 8 semanas. Una vez observado crecimiento en los medios sólidos, se procedió a la identificación utilizando sondas de M tuberculosis complex (Accuprobe, GenProbe, bioMérieux).
Antibioterapia
Estudio con ofloxacino. Ofloxacino se administró por vía oral, 200 mg/12 horas, durante 6 meses. En los tres primeros meses se asoció rifampicina (600 mg/día, oral) e isoniacida (300 mg/día, oral)
Grupo control. Se administró rifampicina (600 mg/día, oral) e isoniacida (300 mg/día, oral) durante los seis meses que duró el tratamiento. Durante los dos primeros meses se asociaron pirazinamida (25 mg/kg/día, oral) y etambutol (25 mg/kg/día, oral).
Seguimiento microbiológico
Durante el tratamiento se llevó a cabo procesándose mensualmente tres muestras de orina matutinas. Una vez finalizado el tratamiento se realizaron controles microbiológicos a los 6 meses y cada año después de la finalización del tratamiento.
Controles clínicos
Los estudios básicos incluyeron: perfil sanguíneo completo, pruebas de función renal y hepática, radiografía de tórax y urograma endovenoso. Las pruebas sanguíneas se repitieron cada mes, al igual que las de la función renal y hepática. El urograma intravenoso se repitió a los 3 y 6 meses de tratamiento.
Determinación de la sensibilidad de M tuberculosis
A ofloxacino
La prueba de sensibilidad a ofloxacino (DL 8280 Hoechst-Roussel, ahora Aventis) se determinó en Mycobacteria 7H11 agar (Difco, Detroit), suplementado con Middlebrook OADC enrichment (Difco). En primer lugar, se preparó una solución madre con 10 mg de ofloxacino que se disolvieron en 0.3 ml de NaOH 0.1 N, añadiendo a continuación 9.4 ml de H2O, y finalmente 0.3 ml de ClH 0.1 N, con lo que se obtuvo una solución de 1000 mcg/ml, con un pH de 5.8. Dicha solución se diluyó de forma adecuada con agua, añadiéndose asépticamente al medio antes esterilizado, para conseguir las concentraciones críticas de 1 y 4 mcg/ml. Los medios, con los antibióticos, se distribuyeron en tubos de tapón de rosca, solidificándolos en posición inclinada. Los inóculos de cada cepa fueron preparados a una turbidez igual a MacFarland nº. 1, diluidos posteriormente al 1/10010. La ausencia de crecimiento en el tubo con la concentración de 1 mcg/ml se interpretó como cepa sensible y el crecimiento a las concentraciones de 1 y 4 mcg/ml, como resistente.
A rifampicina e isoniacida
Se siguió el método de las proporciones de Canetti19. Una cepa se consideró resistente cuando el número de colonias creciendo en el medio con fármacos era superior o igual al 1% del que se apreció en el medio exento de los mismos.
Estudio estadístico
Las diferencias en los resultados entre los regímenes terapéuticos se compararon mediante el programa EPI INFO Versión 6.0 (USD Incorporated, Stone Mountain, Ga, USA). Las proporciones fueron comparadas por el test de chi cuadrado o test exacto de Fisher. La negativización del cultivo fue la variable estudiada. Se consideró que la diferencia entre ambos regímenes era estadísticamente significativa para valores de p<=0.05.
RESULTADOS
Pacientes
Tres pacientes abandonaron el protocolo. Un paciente por embarazo, a los 4 meses de iniciado este. La evolución clínica, analítica y microbiológica durante ese periodo había sido satisfactoria, desarrollándose normalmente tanto la gestación como el parto. Otro paciente presentó una hepatopatía aguda al inicio del protocolo y se decidió excluirle de este. El tercer paciente fué excluído al inicio del protocolo, por falta de colaboración. La evolución de los restantes pacientes fue satisfactoria, remitiendo los síntomas una vez comenzado el tratamiento, siendo muy positiva la colaboración de todos ellos, así como la tolerancia a la medicación.
Estudios y seguimiento microbiológico
La aplicación del protocolo exigía un diagnóstico microbiológico. El cultivo fue positivo en los 29 pacientes (62% con un número de colonias mayor de 100). La tinción fue positiva en 16 pacientes (56%), (Tabla 2). Todas las cepas de M tuberculosis aisladas fueron sensibles a los antibióticos antituberculosos estudiados.
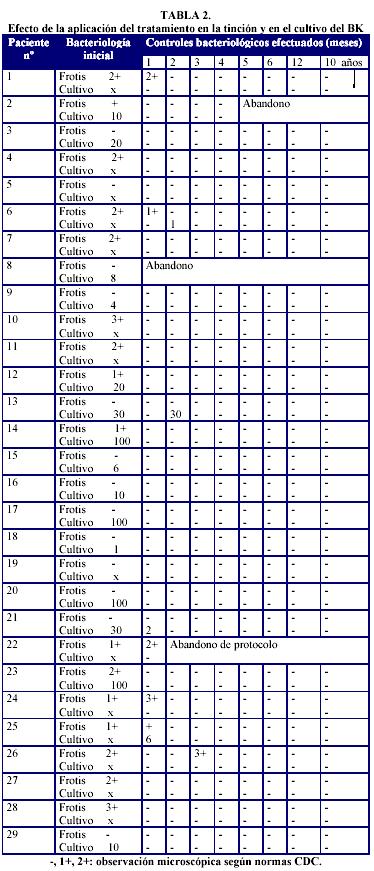
Se observaron cultivos positivos en el primer mes en los pacientes 21 y 25, con 2 y 6 colonias respectivamente, y en el segundo mes en los pacientes 6 y 13 con 1 y 30 colonias respectivamente. Frotis positivos con bacilos ácido alcohol resistentes se observaron en el primer mes de tratamiento en cinco pacientes (1,6, 22, 24 y 25) y en el tercer mes en el paciente 26. Ulteriores exámenes fueron negativos.
Evaluación clínica
No se evidenciaron cambios en el hemograma o en la función renal durante el seguimiento. Las transaminasas de 5 pacientes (17.2%) se incrementaron durante los primeros 3 meses de tratamiento, normalizándose cuando se retiraron rifampicina e isoniacida. Asimismo, 6 pacientes (20.7%) presentaron una elevación de su velocidad de sedimentación eritrocitaria (VSE), normalizándose posteriormente (Tabla 3).

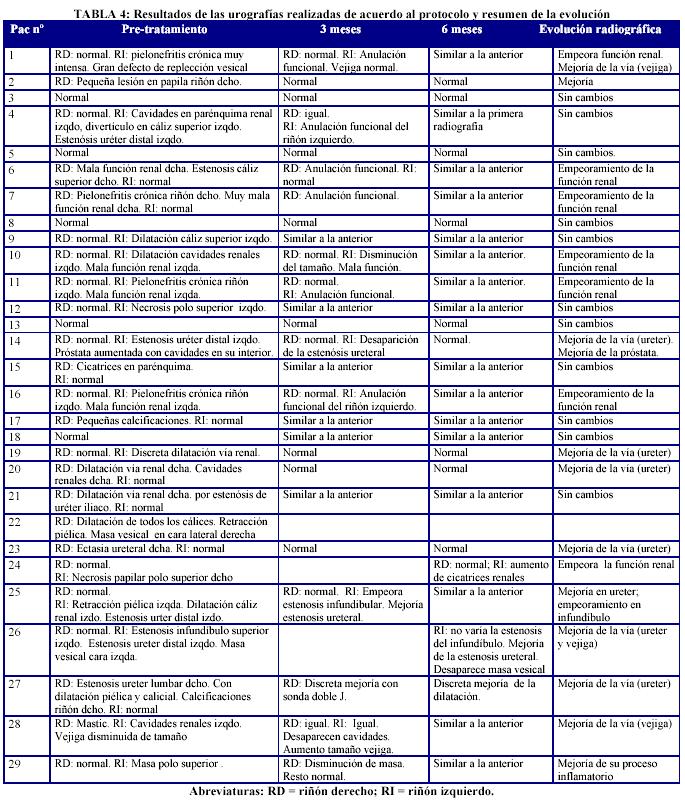
En la Tabla 4 se observan los resultados de las urografías realizadas al inicio del tratamiento y a los 3 y 6 meses. La columna de la derecha resume los datos de la evolución radiográfica. 12 (39.3%) pacientes no experimentaron cambios, otros 11 (39.6%) experimentaron mejoría y 6 (21.4%) mostraron un empeoramiento de su función renal.
Conversión bacteriológica y comparación entre los dos grupos
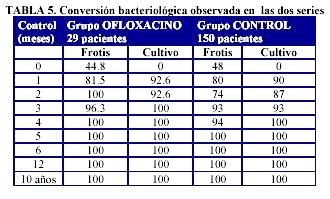
Una vez iniciado el tratamiento, la conversión bacteriológica de los cultivos (negativización) en el grupo tratado con ofloxacino fue del 92.6% el primero y segundo mes, y del 100% a partir del tercer mes. En el grupo control de 150 pacientes, asimismo con TBU, la conversión fue del 90% el primer mes, 87% el segundo y 93% el tercero. A partir del cuarto mes la conversión fue del 100%. La evolución de los frotis y de los cultivos de ambas series se describe en la Tabla 5.
DISCUSIÓN
Varios son los puntos que deben considerarse en esta discusión: actividad frente a M tuberculosis de las quinolonas fluoradas (especialmente ofloxacino), biodisponibilidad del producto, tolerancia, interacciones con otros fármacos antituberculosos, valoración bacteriológica y clínica e impacto presente y futuro de esta pauta terapéutica, y de las quinolonas en general, en el tratamiento de la tuberculosis urinaria.
Con relación a la actividad in vitro, esta es buena frente a cepas de M tuberculosis, constituyendo uno de los grupos mas prometedores en este campo20-22. En nuestro caso, todas las cepas se mostraron sensibles a isoniacida y rifampicina. Las concentraciones mínimas inhibitorias (CMIs) observadas a ofloxacino fueron inferiores a 1 mcg/ml, similares a las referidas por otros autores23-24. Asimismo, todas las cepas de M tuberculosis se mostraron sensibles a isoniacida y rifampicina. La biodisponibilidad por vía oral de ofloxacino es excelente. La posología de 200 mg cada 12 horas, unido a la farmacocinética favorable, permite conseguir unas concentraciones medias en orina que superan ampliamente aquellas CMIs25.
Sin duda, la búsqueda de nuevas sustancias para el tratamiento de la tuberculosis debe de perseguir la colaboración del paciente. Al igual que otros autores26, consideramos que un régimen corto con antibióticos bien tolerados evita el abandono del tratamiento, los fracasos y el incremento de los niveles de resistencia primaria en el entorno27. Por ello, la utilización de este tratamiento corto pretendió paliar parte de los inconvenientes observados en las pautas establecidas, sin menoscabo de la eficacia terapéutica, basándose en las propiedades de la quinolona ofloxacino28.
Una situación que se debe de tener en cuenta es la posible interacción con otros fármacos antituberculosos. Así, es conocida la acción inhibitoria de las quinolonas fluoradas sobre el sistema citocromo P-450 (CYP450) que puede acarrear una interacción negativa con rifampicina29. Sin embargo, aunque este hecho ha sido puesto de manifiesto frente a ciprofloxacino, no existe constancia de que se presente con ofloxacino. Por ello, la ausencia de resistencias cruzadas, y la posibilidad de un efecto sinérgico con los antibióticos antituberculosos utilizados, constituyeron una situación de partida prometedora30. Últimamente, se han descrito cepas de M tuberculosis resistentes a ofloxacino, derivados de un posible mal uso de la misma31.
Por otra parte, la utilización de isoniacida y rifampicina en los tres primeros meses de tratamiento, creemos que fue fundamental debido a la rápida acción esterilizante de las lesiones, eliminando tanto la población extracelular como aquella presente en las lesiones cerradas y en los macrófagos16, 32.
En este estudio de seguimiento, todos los pacientes se curaron, sin observarse recaídas ulteriores. Consideramos asimismo que, en dos de los pacientes que se retiraron del protocolo, no hubo razones objetivas para atribuir toxicidad hepática, renal, hematológica ni efectos teratógenos a ofloxacino33.
Aunque la negativización de los esputos en los casos de tuberculosis pulmonar se suele conseguir, de acuerdo a algunos autores en dos meses cuando el régimen terapéutico incorpora INH y RMP, no se poseen datos concretos con respecto a la tuberculosis genitourinaria. Nuestros resultados, con la terapia que incorpora ofloxacino, señalan que, a partir del tercer mes, se alcanza el 100% de negativización. No obstante, se evidencian controles bacteriológicos positivos en el seguimiento, aislándose colonias de M tuberculosis, en el primer mes (dos pacientes) con menos de 6 colonias y en el segundo mes (dos pacientes) con 1 y 30 colonias respectivamente. Conviene señalar, con respecto a los frotis, la visualización de bacilos ácido alcohol resistentes en el primer control en cinco pacientes y en el tercer mes en un paciente. En ninguno de estos pacientes se aislaron cepas de M tuberculosis, ya que, de acuerdo con nuestra experiencia, estos se negativizan mas lentamente que los cultivos.
El seguimiento cuidadoso de los pacientes a lo largo de más de una década, sin incidentes reseñables, pone de manifiesto la bondad del esquema terapéutico presentado. Por ello no resulta extraño que al compararlo con el grupo control, no se observen diferencias significativas.
Sin duda, son necesarios estudios más amplios que incluyan las nuevas alternativas terapéuticas que puedan aportar, en iguales condiciones de eficacia, mejoras que eviten los efectos adversos de los medicamentos y que potencien el grado de colaboración de los pacientes34. Asimismo, conviene tener presente que, en este régimen terapéutico, se establece una monoterapia a lo largo de la mitad del mismo. Si el poder esterilizante de dos fármacos antituberculosos (RMP e INH) es fundamental en los inicios del tratamiento, la actuación de ofloxacino puede culminar posteriormente la misma. Creemos que se puede abrir una nueva perspectiva terapéutica, la cual, aunque novedosa de acuerdo a las referencias bibliográficas revisadas, basa su eficacia en el uso controlado de ofloxacino, en el seguimiento cuidadoso de los pacientes a lo largo de un tiempo prolongado, y en la conversión bacteriológica de los cultivos de M tuberculosis que son una prueba de la eficacia del régimen utilizado.
La disponibilidad de las actuales quinolonas, más potentes, perfila un nuevo escenario en el tratamiento de la tuberculosis, especialmente la genitourinaria. Las dudas que se cernían hace dieciocho años sobre la eficacia real de este régimen expuesto, desde algunos sectores sanitarios, deberían de quedar esclarecidos al observar la evolución y buena colaboración de los pacientes. En conclusión, la utilización de esta o de otras quinolonas abre una vía de nuevas posibilidades terapéuticas, las cuales, sin duda, pueden aportar ventajas en todas las formas de tuberculosis, incluyendo aquellas en las que se aíslen cepas multirresistentes y que constituyen una seria amenaza en el momento actual.
Agradecimientos
Los autores agradecen al Dr M Gonzalez Sagrado de la Unidad de Investigación del HU Río Hortega, la colaboración en la redacción del trabajo.
REFERENCIAS
1. Ziganshina LE, Vizel AA, Suire SB. Fluoroquinolonas para el tratamiento de la tuberculosis (Rev Cochrane traducida). En: La Biblioteca Cochrane Plus, 2005 Número 4. Oxford: Update Software Ltd.
2. Grupo de trabajo del PMIT. La tuberculosis en España: resultados del Proyecto Multicéntrico de Investigación sobre Tuberculosis (PMIT). Madrid: Ed. Instituto de Salud Carlos III, 1999.
3. Bass JB, Farer LS, Hopewell PC et al. Treatment of tuberculosis and tuberculosis infection in adults and children. Am J Respir Crit Care Med 1986; 134:355-358.
4. Lenk S, Schoeder J. Genitourinary tuberculosis. Curr Opin Urol 2001; 11:93-98.
5. Ortega S, March J. Tratamiento de las infecciones por micobacterias. In: García Sanchez JE, López R, Prieto J, editors. Antimicrobianos en medicina. Sociedad Española de Quimioterapia. Barcelona, Philadelphia: Prous Science, 1999; p. 661-667.
6. Jain VK, Vardhan H, Prakash OM. Pyrazinamide induced thrombocytopenia. Tubercle 1988; 69: 217-218.
7. Rodriguez JC, Ruiz M, Lopez M, Royo G. In vitro activity of moxifloxacin, levofloxacin and linezolid against Mycobacterium tuberculosis. Int J Antimicrob Agents 2002; 20:464-467.
8. Sumartejo E. When tuberculosis teatment fails. A social behavioral account of patient adherence. Am Rev Respir Dis 1993; 147:1311-1320.
9. Casal M, Gutierrez J, Gonzalez J, Ruiz P In vitro susceptibility of Mycobacterium tuberculosis to ofloxacin and ciprofloxacin in combination with rifampin and isoniazid. Chemioterapia 1987; 6: 437-439.
10. García-Rodriguez JA. Activity of quinolones against Mycobacteria in vitro and in vivo. Quinolones Bulletin 1988; 4: 21-25.
11. Casal M, P Ruiz, A Herreras and the Spanish study Group of M tuberculosis resistance. Study of the in vitro susceptibility of M tuberculosis to ofloxacin in Spain. Int J Tuberc Lung Dis 2000; 4: 588-591.
12. Tsukamura M. In vitro antituberculosis activity of a new antibacterial substance Ofloxacin (DL 8280). Am Rev Respir Dis 1985; 131:348-351.
13. Shah PM, Frech K. Clinical experiences with quinolones. Overview. Quinolones Bulletin 1985;1:19-21.
14. Tsukamura M, E Nakamura, S Oshii and H Amano. Therapeutic effect of a new antibacterial substance ofloxacin (DL-8280) on pulmonary tuberculosis. Am Rev Respir Dis 1985; 131: 352-356.
15. AK Dutt, Stead WW. Chemotherapy of tuberculosis for the 1980`s. In: Stead WW and Dutt AK, editors. Clinics in Chest Medicine-Tuberculosis. Philadelphia: WB Sanders Company; 1980; p. 243-52.
16. Grassi C, Peona V. New drugs for tuberculosis. Eur Respir J 1995; 8(Suppl 20): S714-8.
17. Ginsburg AS, Grosset JH, Bishai WR. Fluoroquinolones, tuberculosis and resistance. Lancet Infectious Diseases 2003; 3: 432-42.
18. Metchock BG, Nolte FS, Wallace RJ. Mycobacterium. In: Murray P, Baron EJ, Pfaller MA, Tenover FC, Yolken RH, editors. Manual of Clinical Microbiology. 7th ed. Washington: American Society for Microbiology, 1999; p. 399-437.
19. Canetti G, Rist N, Grosset J. Mesure de la sensibilité du bacille tuberculeux aux drogues antibacillaires par la méthode des proportions. Méthodologie, critères de résistance, résultats, interprétation. Rev Tub Pneum 1963; 27:217-72.
20. Jacobs MR. Activity of quinolones against mycobacteria. Drugs 1995; 49 (Suppl.2):67-75.
21. Tomioka H. Prospects for development of new antimycobacterial drugs. J Infect Chemother 2000; 6: 8-20.
22. Coll P. Fármacos con actividad frente a Mycobacterium tuberculosis. Enferm Infecc Microbiol Clin 2003; 21: 299-308.
23. Rastogi N, Goh KS, Bryskier A, Devallois A. In vitro activities of levofloxacin used alone and in combination with first- and second-line antituberculous drugs against Mycobacterium tuberculosis. Antimicrob Agents Chemother 1996; 40:1610-6.
24. Yew WW, Kwan SY, Ma WK, Khin MA, Chau PY. In vitro activity of ofloxacin against Mycobacterium tuberculosis and its clinical efficacy in multiply resistant pulmonary tuberculosis. J Antimicrob Chemother 1990; 26:227-36.
25. Stambaugh JJ, Berning SE, Bulppitt AE, Hollender ES, Narita M, Ashkin D, Peloquin CA. Ofloxacin population pharmacokinetics in patients with tuberculosis. Int J Tuberc Lung Dis 2002; 6: 503-509.
26. Ledru S, B Cauchoix, M Yaméogo, A Zoubga, J Lamandé-Chiron, F Portaels, JP Chiron. Impact of short-course therapy on tuberculosis drug resistance in South-West Burkina Faso. Tubercle and Lung Disease 1996; 77: 429-436.
27. Alberte-Castiñeiras A, Brezmes-Valdivieso MF, Campos-Bueno A, Montes-Martínez I, López-Medrano R, Avellaneda C, Pérez-Pascual P, Della-Latta P. Drug-resistant tuberculosis in Castilla-León, Spain, 1996-2000. Int J Tuberc Lung Dis 2006; 10: 554-558.
28. Alegre J, Fernández de Sevilla T, Falco V, Martínez Vazquez JM. Ofloxacin in miliary tuberculosis. Eur Respir J 1990; 3:238-9.
29. Berning SE. The role of fluoroquinolones in tuberculosis today. Drugs 2001; 61: 9-18.
30. Yew WW, Chan CK, Chau CH, Tam CM, Leung CC, Wong PC, Lee I. Outcomes of patients with multidrug-resistant pulmonary tuberculosis treated with ofloxacin/levofloxacin-containing regimens. Chest 2000; 117: 744-751.
31. Ruiru Shi, Jianyuan Zhang, Chuanyou Li, Yuko Kazumi and Isamu Sugawara. Emergence of ofloxacin resistance in Mycobacterium tuberculosis clinical isolates from China as determined by gyrA mutation analysis using denaturing high-pressure liquid chromatography and DNA sequencing. J Clin Microbiol 2006; 44: 4566-4568.
32. Rastogi N, Labrouse V, Goh KS. In vitro activities of fourteen antimicrobial agents against drug susceptible and resistant clinical isolates of Mycobacterium tuberculosis and comparative intracellular activities against the virulent H37Rv strain in human macrophages. Current Microbiology 1996; 33: 167-175.
33. Saigai S, Agarwai SR, Nandeesh HP and Sarin SK. Safety of an ofloxacin-based antitubercular regimen for the treatment of tuberculosis in patients with underlying chronic liver disease: a preliminary report. Journal of gastroenterology and Hepatology 2001; 16: 1028-1032.
34. Valerio G, Bracciale P, Manisco V, Qitadamo M, Legari G, Bellanova S. Long-term tolerance and effectiveness of moxifloxacin therapy for tuberculosis: preliminary results. J Chemother 2003; 15: 66-70.
Correspondencia:
Armando Alberte Castiñeiras. Microbiología. Hospital del Río Hortega, 47010 Valladolid
aalberte @ hurh.sacyl.es
