Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
Letters to the Editor / Cartas al Editor
VIGILANCIA POSTCOMERCIALIZACION DE REACCIONES ADVERSAS ASOCIADAS A CAPTOPRIL Y ENALAPRIL. CUBA 2005 - 2009.
Ashley Chao Cardeso1, Ivette Díaz Mato2, Giset Jiménez López1, Ismary Alfonso Orta1, Jenny Ávila Pérez1, Gilberto Piedra Ruiz3
1Unidad Coordinadora Nacional de Farmacovigilancia. Centro para el Desarrollo de la Farmacoepidemiología.
2 Facultad de Ciencias Médicas: "Dr. Salvador Allende". Ciudad Habana.
3Hospital General Docente: "Enrique Cabrera".
Cuba.
ashleychao77 @ yahoo.com
Rev Electron Biomed / Electron J Biomed 2010;3:67-70
Sr. Editor:
Los Inhibidores de la Enzima Convertidora de Angiotensina (IECA) constituyen un grupo de fármacos ampliamente utilizados en la terapéutica de enfermedades cardiovasculares. Son la piedra angular del tratamiento de la Insuficiencia Cardiaca en todas sus fases de severidad. Se consideran de primera elección en pacientes con disfunción ventricular izquierda luego de un infarto del miocardio, y además, poseen demostrada eficacia antihipertensiva así como en la progresión de la nefropatía diabética en hipertensos1-4.
Producen vasodilatación arteriovenosa, con la consecuente disminución de la resistencia vascular periférica y aumentan la capacitancia venosa. Dichas acciones favorecen la disminución de la pre y post carga cardiaca. Esto se debe, a que los IECA inhiben la síntesis de Angitensina ll, vasoconstrictor potente que estimula a los receptores AT1 localizados en la musculatura lisa de vasos sanguíneos; incrementa la acción de la noradrenalina a nivel de terminaciones nerviosas simpáticas e inhibe su recaptación e inactivación a nivel neuronal, favorece el remodelamiento vascular, cardiaco, y estimula la liberación de aldosterona y la retención hidrosalina en el organismo1-4.
A pesar de las diferencias farmacocinéticas que poseen los IECA, todos comparten efectos farmacológicos, aplicaciones terapéuticas, reacciones adversas (RAM), y contraindicaciones similares. Desde el punto de vista químico, se pueden agrupar de la siguiente manera1-4. Sulfidrílicos Carboxílicos Fosfóricos Captopril Enalapril Fosinopril Alecepril Ramipril Ceranapril Zofenopril Espirapril - - Trandolapril - - Lisinopril -
En Cuba, se dispone del captopril, que se presenta en tabletas de 25 y 50 miligramos (mg), y el enalapril, cuyos comprimidos son de 10 y 20 mg5.
Teniendo en cuenta que las enfermedades cardiovasculares en nuestro país ocupan la primera causa de muerte, y que los IECA, son muy utilizados en el tratamiento de estas patologías, se decidió realizar una revisión en la Base de Datos Nacional de Farmacovigilancia, con el objetivo de caracterizar las RAM notificadas a la Unidad Coordinadora Nacional de Farmacovigilancia (UCNFv) en el período comprendido desde enero - 2005 hasta diciembre - 2009, identificar los grupos etáreos más afectados y las RAM más notificadas, así como clasificarlas según severidad.
Hemos realizado un estudio descriptivo, transversal y retrospectivo de Farmacovigilancia utilizando el método de notificación espontánea. Consistió en el análisis de las Sospechas de RAM (SRAM) asociadas a los IECA de producción nacional (captopril y enalapril) que fueron notificadas a la UCNFv en el período comprendido desde enero, 2005- diciembre, 2009.
Universo: total de SRAM a medicamentos. Período: enero, 2005- diciembre, 2009.
Muestra: total de SRAM por captopril y enalapril en el período comprendido desde enero, 2005- diciembre, 2009.
Criterios de exclusión: se excluyeron las SRAM a otros grupos de medicamentos.
La información se obtuvo fundamentalmente de la Base de Datos Nacional de Farmacovigilancia que aportó la información concerniente a los reportes de SRAM por captopril y enalapril.
En la actualidad, se emplean diversos criterios de clasificación de RAM:
De acuerdo a la gravedad se agrupan en leves, moderadas, graves y mortales. Este criterio de clasificación se basa en el análisis de la necesidad de hospitalización o no del paciente, si la RAM o efecto indeseable requirió cambio de terapia o antídototerapia. Se evalúa si puso en peligro la vida y si contribuyó como causa directa o indirecta a su muerte6.
Según la asociación causal pueden ser definitivas o definidas, probables, posibles, condicionales y no relacionadas. En este caso, se emplean algoritmos de causalidad o imputabilidad. En Cuba se usa el de Karch y Lasagna (Anexo 1). Se evalúa la secuencia temporal plausible en relación con la administración del medicamento y la aparición de la RAM, la posible explicación del efecto indeseable por causas alternativas (otros fármacos, enfermedad de base, entre otros). Se debe tener en cuenta, la respuesta del paciente al retirarle el medicamento y si hubo reaparición de los síntomas tras la re- exposición al mismo6.
Se aplicaron técnicas de estadística descriptiva para cada variable. Los principales resultados se presentan en tablas para facilitar una mejor comprensión de los mismos.
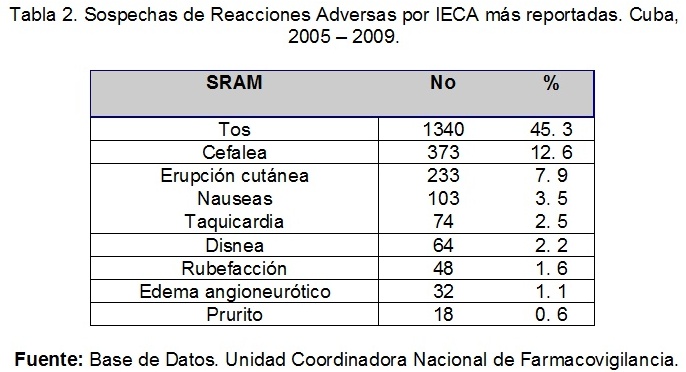
En la tabla 2, se puede observar que la RA más reportada fue la tos (45.3%), la cefalea y erupciones cutáneas ocuparon el segundo y tercer lugar respectivamente.
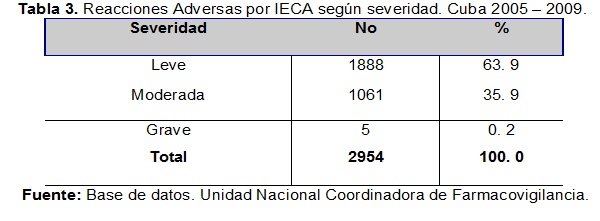
Existió un predominio de RA leves (tabla 3), seguido de las moderadas (35.9 %).

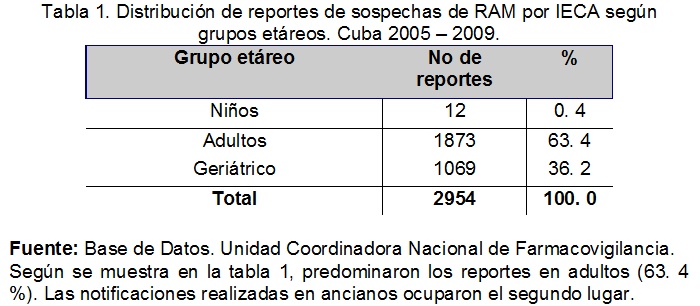
Como se puede observar en la tabla 1, predominaron los reportes en adultos (63.4%). Este hecho es justificable, pues, el mayor número de SRAM que se notifican a la UCNFv corresponde a este subgrupo poblacional. No son despreciables las notificaciones realizadas en ancianos, las cuales ocuparon un 36. 2%. Los pacientes geriátricos son más sensibles a presentar eventos cardiovasculares por IECA, principalmente la hipotensión ortostática, la cual suele aparecer al inicio del tratamiento1-3 por lo que debe iniciarse con bajas dosis, para evitar o minimizar la aparición de este efecto indeseable.
La RAM más reportada fue la tos. Esta puede ser explicada por el mecanismo de acción de los IECA, pues, la enzima convertidora, no solo es la responsable de la síntesis de Angiotensina ll, paralelamente degrada a la bradiquinina, que es un excelente mediador proinflamatorio. La inhibición farmacológica de esta enzima favorece la acumulación de dicha sustancia en el sistema respiratorio y puede causar tos seca y molesta entre el 5 y el 20 % de los pacientes tratados. Es más frecuente en mujeres y por lo general no depende de la dosis administrada. En ocasiones obliga a suspender la medicación3-5.
La cefalea y la rubefacción pueden ser consecuencia de la vasodilatación que ocasionan estos agentes. La inhibición de la síntesis de Angitensina ll (potente vasoconstrictor) y de la degradación de bradiquinina (importante vasodilatador) pudieran explicar el hecho anterior. Además se reportaron 74 taquicardias, las cuales son predecibles y esperables (tipo A). El aumento de la frecuencia cardiaca es resultante de un mecanismo reflejo compensador por la disminución de la Resistencia Vascular Periférica y de la Presión Arterial3-4.
No son nada despreciables las reacciones alérgicas notificadas: erupciones cutáneas, prurito, disnea, edema angioneurótico, entre otros. Estas RAM aparecen descritas en el Formulario Nacional de Medicamentos (FNM) para estos productos5. Son de hipersensibilidad, tipo B, no pueden explicarse por la acción del medicamento ni son predecibles, y la severidad de las mismas no depende de la dosis administrada6-8.
El edema angioneurótico (inflamación rápida de nariz, faringe, lengua, labios), es una complicación infrecuente que puede llegar a comprometer la vida del paciente. Suele aparecer en las primeras semanas de iniciado el tratamiento con IECA. Aunque no se puede explicar claramente el mecanismo por el cual se produce, pudiera deberse a acumulación de bradiquinina, inducción de anticuerpos específicos, o a inhibición de la inactivación del complemento 1- esterasa. Cuando se instaura este cuadro, se debe suprimir inmediatamente el fármaco y administrar adrelanina, un antagonista de receptores H1 y/o glucocorticoides8.
No se reportaron RAM a IECA en embarazadas, pues en Cuba no se prescriben estos fármacos durante la gestación. Su empleo induce incremento en la incidencia de malformaciones congénitas cardiacas fetales, descenso de la función renal, oligohidramnios, retardo en la osificación craneal, así como insuficiencia renal, hipotensión e hiperpotasemia en neonatos9-10.
En cuanto a la severidad, predominaron las RAM leves y moderadas, resultados que concuerdan con lo reportado en otros estudios de Farmacovigilancia11-12. Estas últimas son las que requieren atención médica de urgencias, cambio del tratamiento farmacológico y/o antídototerapia. Las graves ocuparon un 0.2 % (5 reportes): 4 al captopril que incluyeron 2 dolores precordiales, 1 melena, las cuales son RAM no descritas al medicamento5,9. y además se reportó 1 edema. Al enelapril se notificó 1 hipotensión arterial, que fue considerada según imputabilidad como posible, pues, además de aparecer descrita en el FNM, el paciente tenía incluido en su tratamiento otros fármacos antihipertensivos que podrían explicar esta RAM. No se reportó ninguna mortal.
Se concluye que el mayor número de reportes de RA por IECA afectó a la población adulta. Tal y como se esperaba la reacción más reportada fue la tos. El comportamiento en cuanto a severidad coincidió con lo reportado en la literatura, pues predominaron las reacciones leves.
REFERENCIAS
- 1.- Borroto Regalado R. Insuficiencia cardiaca. En: Morón N, Ed. Farmacología Clínica. Ed. La Habana: ECIMED, 2008: 159 - 182. Disponible en: http://www.bvs.sld.cu/libros_texto/farmacologia_clinica/cap8.pdf
2.- Goodman & Gilman's the pharmacological basis of therapeutics (CD-ROM) - 11th ed. (2006).
3.- Borroto Regalado R. Fármacos utilizados en el tratamiento de la Insuficiencia Cardiaca. En: Vergel-Tasé-Groning. Farmacología. Proceso de Atención de Enfermería. Ed. La Habana: ECIMED, 2009: 193 - 211. Disponible en: http://www.bvs.sld.cu/libros_texto/farmacologia. proceso de atencion de enfermeria/cap12.pdf
4.- Furones Mourelle JA. Hipertensión Arterial. En: Morón N, Ed. Farmacología Clínica. Ed. La Habana: ECIMED, 2008: 133 - 158. Disponible en: http://www.bvs.sld.cu/libros_texto/farmacologia_clinica/cap7.pdf
5.- Colectivo de de autores. Formulario Nacional de Medicamentos. Centro para el desarrollo de la Farmacoepidemiología. MINSAP. Editorial Ciencias Médicas. Cuba. 2006. disponible en: http://www.cdf.sld.cu/completo.pdf
6.- Chao A, Díaz I, Jiménez G, López Y, Fernández X. Análisis de las sospechas de reacciones adversas producidas por analgésicos no opioides. Cuba 2007. Botín Fármacos, Vol. 12 (2). Disponible en: http://www.boletinfarmacos.org
7.- Pérez Hernández B. Reacciones adversas a los medicamentos y adicción a otras sustancias. En: Morón - Levy N, ed. Farmacología General. Ed. La Habana: ECIMED, 2002:124-137.
8.- De Cas Florez J. Reacciones adversas a los medicamentos. En: Flórez J, S ed. Farmacología Humana. Navarra: Ediciones universitarias de Navarra, SA, 2003:155- 166.
9.- Comunicación sobre Riesgos de medicamentos para profesionales sanitarios: Inhibidores de la enzima convertidora de angiotensina (IECA) y antagonistas de los receptores de angiotensina II (ARAII): Actualización de información por riesgos de su uso durante el embarazo. Espańa. Disponible en: http://www.agemed.es/actividad/alertas/usoHumano/seguridad/angiotensinaII-abril08.htm
10.- Cooper WO et al., Major congenital malformations after first-trimester exposure to ACE inhibitors, N Engl J Med 2006; 354(23):243- 51
11.- Legón T, Jiménez G, Alfonso I, Díaz I, Chao A. Seguridad del paracetamol en Cuba. 2003 - 2008. Rev Electron Biomed / Electron J Biomed 2010;2:25-32. Disponible en: http://biomed.uninet.edu/2010/n2/legon.html
12.- Zapata Martínez A. Farmacovigilancia. En: Morón-Levy N, Ed. Farmacología General. Ed. La Habana: ECIMED, 2002: 139 - 146.
Correspondencia:
Ashley Chao Cardeso
Unidad Coordinadora Nacional de Farmacovigilancia. Centro para el Desarrollo de la Farmacoepidemiología.
Ciudad Habana. Cuba.
ashleychao77 @ yahoo.com
Recibido 17 de diciembre de 2010.
Publicado: 23 de diciembre de 2010
