Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
- Aleatorización apropiada
- Enmascaramiento de la asignación
- Cegamiento de la intervención
- Seguimiento completo
- Cegamiento de la medición de resultados
VALOR DEL ESTRONCIO EN LA PREVENCIÓN DE FRACTURAS ÓSEAS SECUNDARIAS A CAÍDAS EN PERSONAS MUY ANCIANAS PORTADORAS DE OSTEOPOROSIS PRIMARIA:
UNA REVISIÓN SISTEMÁTICA
Carlos G. Musso, Ricardo Jáuregui, Agustín Ciapponi
Centro Médico Agustin Rocca. Hospital Italiano de Buenos Aires. Argentina
carlos.musso @ hospitalitaliano.org.ar
Rev Electron Biomed / Electron J Biomed 2011;1:60-67.
Comentario del revisor Dr. Hugo Alberto Schifis. Presidente de la Sociedad Argentina de Gerontología y Geriatría. Facultad de Ciencias Médicas de la Universidad de Buenos Aires. Argentina..
Comentario del revisor Dr. Ignacio Martínez Sancho MD. Médico de Familia. Centro de Salud "Gamonal Antigüa". Burgos, España.
RESUMEN
Introducción: dado que entre el 25-30% de las fracturas óseas, y 60% de las fracturas de cadera de la población general, acontecen en el subgrupo correspondiente a las mujeres muy ancianas. Esto se debe a la alta prevalencia de osteoporosis primaria e incidencia de caídas característica de este grupo, hemos decidido investigar el valor del estroncio en la prevención de fracturas óseas secundarias a caídas en personas muy ancianas portadoras de osteoporosis primaria por medio de una revisión sistemática de la bibliografía.
Material y Métodos: se realizó una revisión sistemática de la literatura siguiendo las recomendaciones de la metodología Cochrane. De los 8 los documentos inicialmente recuperados, sólo 2 terminaron siendo incluidos (2 revisores independientes, seleccionaron evaluaron y extractaron los datos de los estudios incluidos) por ser los únicos que cumplían con el criterio de elegibilidad de ser estudios realizados sobre una población de pacientes muy ancianos: mayor de 74 años de edad, totalizando 2616 personas en estudio.
Resultados: a pesar la abundancia de datos a favor del tratamiento con estroncio, hay un riesgo relativo para fractura no vertebral al año de tratamiento que pasa por la unidad: 0.58 [0.32, 1.06]. En cuanto al riesgo de fractura a nivel de la cadera, existe ciertas diferencias respecto de los datos antes mencionados. Por un lado, la reducción del riesgo de fractura (32%) luego de 3 años de tratamiento con ranelato de estroncio documentada por el estudio Seeman 2006 no alcanzó significación estadística (p=0.112), y su riesgo relativo pasa por la unidad: 0.68 [0.45, 1.05]
Sin embargo, el estudio Reginster 2008 demostró luego de 5 años de tratamiento con ranelato de estroncio una reducción mayor (43%) y estadísticamente significativa (p=0.036).
Estos datos podrían significar que tal vez el hueso de la cadera requiera un tiempo de exposición más prolongado al estroncio para verse beneficiado en una efectiva reducción de su riesgo de fractura.
Conclusiones: la mayor reducción del riesgo de fractura se vio en fracturas vertebrales respecto de las no vertebrales, si bien los IC 95% se superponen ampliamente. Así mismo, el mayor efecto anti-fractura se documento luego del año de tratamiento con ranelato de estroncio respecto de los 3 años del mismo, así como también se documento una mayor reducción del riesgo de fractura a los 3 años de tratamiento respecto de los 5 años del mismo. Concluimos que hay pruebas que apoyan la utilidad del ranelato de estroncio, en dosis de 2 gramos diarios suministrado durante al menos 3 años, para reducir significativamente la incidencia de fracturas vertebrales y no vertebrales en mujeres muy ancianas con osteoporosis primaria.
PALABRAS CLAVE: Estroncio. Fracturas. Osteoporosis.
SUMMARY: VALUE OF STRONTIUM IN THE PREVENTION OF BONE FRACTURES CAUSED BY FALLS IN VERY OLD PATIENTS WHO SUFFER FROM PRIMARY OSTEOPOROSIS: A SYSTEMATIC REVISION.
Introduction: Since between 25-30% bone fractures, and 60% hip fractures in the general population are common in the subgroup which correspond to very old women. This happens due to the high predominance of primary osteoporosis and the incidence of falls which are characteristic of such group; thus, we have decided to investigate, through a systematic revision of the bibliography, the value of strontium in the prevention of bone fractures caused by falls in very old patients who suffer from primary osteoporosis.
Material and Method: A systematic revision of the literature was carried out following the recommendations of the Cochrane methodology. Out of the 8 documents initially recovered, only two were included (2 independent reviewers selected, evaluated and extracted the data from the included tests) since such tests were the only ones which complied with the eligibility criteria to be tests performed on a population of very old patients: older than 74 years old, thus reaching a total amount of 2616 patients who took part in this test.
Results: Despite the abundance of information in favour of the treatment using strontium, there is a relative risk in the case of non-vertebral fractures one year after treatment which goes through unit: 0.58 [0.32, 1.06]. Regarding the risk of fracture at the hip level, there are certain differences when it is compared with the aforementioned data. On the one hand, the reduction of the risk of fractures (32%) after 3 years of treatment with strontium ranelate documented by the Seeman test 2006 did not reach statistical significance (p=0.112), and its relative risk goes through unit: 0.68 [0.45, 1.05]
Nevertheless, the Reginster 2008 test showed that after 5 years of treatment with strontium ranelate there was a bigger reduction (43%) which was statistically significant (p=0.036) (Tables 1 and 4).
Such data could mean that the hip bone may need a longer period of exposure to strontium to benefit from an effective reduction of its risk of fracture.
Conclusions: The biggest reduction in the risk of fracture was evidenced in vertebral fractures compared with the non vertebral fractures, even when the IC 95% overlap significantly. Additionally, the biggest anti-fracture effect was documented one year after treatment using strontium ranelate in comparison with the 3 years of the same treatment, as well as a bigger reduction in the risk of fracture after 3 years compared with five years of it. We conclude that there are tests that support the use of strontium ranelate, in 2 grams doses administered daily for at least 3 years, to achieve a significant reduction of the incidence of vertebral as well as non vertebral fractures in very old women with primary osteoporosis.
KEY WORDS: Strontium. Fractures. Osteoporosis.
INTRODUCCIÓN
Aproximadamente, entre el 25-30% de las fracturas óseas, y 60% de las fracturas de cadera de la población general, acontecen en el subgrupo correspondiente a las mujeres muy ancianas (edad mayor de 75 años). Esto se debe a la alta prevalencia de osteoporosis primaria e incidencia de caídas característica de este grupo1.
La osteoporosis es un trastorno esquelético caracterizado por baja masa ósea y deterioro de la microarquitectura del hueso que provoca aumento de la fragilidad ósea y riesgo de fractura2,3 mientras que la caída como síndrome geriátrico consiste en una complicación propia del trastorno en la marcha característico del anciano.
Dado lo antes mencionado, y el hecho de que este grupo etario va en claro aumento en el mundo occidental, la prevención de esta patología (osteoporosis) y sus complicaciones (fractura ósea, inmovilidad, etc) posee un decisivo impacto económico sobre los presupuestos de los sistemas de salud4.
La fragilidad ósea que caracteriza a la osteoporosis resulta de un desequilibrio en la remodelación ósea: la resorción ósea excede a la formación ósea, y el aumento de la tasa de remodelación a nivel tisular5. En 1994 un grupo de trabajo de la Organización Mundial de la Salud propuso que un individuo con densitometría ósea mayor de 2,5 desviaciones estándar (DE) por debajo de la media de un adulto joven padece osteoporosis6.
El tratamiento farmacológico para la prevención y el tratamiento de esta entidad incluye dos tipos principales de fármacos: agentes antirresorción y anabólicos. Los agentes antiresorción aumentan la resistencia ósea al disminuir la acción osteolítica. Por el contrario, los agentes anabólicos aumentan la resistencia ósea al aumentar la masa ósea debido a un aumento en la actividad osteoblástica7,8.
Sin embargo existe un agente oral nuevo, el ranelato de estroncio, que posee el particular doble beneficio de no sólo ser un inhibidor de la resorción ósea (actividad osteoclástica), sino además un estimulador de formación de dicho tejido (actividad osteoblástica). Desde el punto de vista químico, este producto consta de dos átomos del catión divalente de estroncio estable (elemento natural) y una fracción orgánica (ácido ranélico) que se disocia a nivel gastrointestinal. El estroncio es un catión y está estrechamente relacionado desde el punto de vista físico con el calcio, un componente activo del esqueleto. El ácido ranélico es una molécula orgánica sumamente polar sin actividad farmacológica. Si bien se han probado diferentes dosis de ranelato de estroncio (0.125 - 2 g), se considera a la dosis de 2 gramos diarios como la más recomendada9,10.
En función de todo lo expuesto decidimos investigar el valor del estroncio en la prevención de fracturas óseas secundarias a caídas en personas muy ancianas portadoras de osteoporosis primaria por medio de una revisión sistemática de la bibliografía.
MATERIAL Y MÉTODOS:
Se realizó una Revisión Sistemática, para lo cual procedimos inicialmente a la elaboración de las siguientes preguntas guías recomendadas para la realización de una revisión sistemática de ensayos aleatorizados, doble ciego, controlados que cumplieran con los siguientes criterios de selección:
-
1) Paciente/problema: muy ancianos (edad mayor de 75 años) portadores de osteoporosis (densidad mineral ósea de la columna lumbar de < -2,5 DE). (oldest old/ very old - osteoporosis)
2) Intervención: terapéutica con estroncio 2 gramos/día (strontium) al menos por el lapso de 2 años (además de recibir también calcio 500-1000 mg/día y vitamina D 400-800 UI/día).
3) Comparación: pacientes no tratados con estroncio: placebo (placebo) pero si recibiendo calcio 500-1000 mg/día y vitamina D 400-800 UI/día
4) Resultado (principal evento de interés): fractura (documentada radiológicamente) secundaria a caídas propiciadas por trastorno de la marcha senil (bone fracture - falls)
Se efectuó una búsqueda bibliográfica utilizando como palabras clave: los ítems antes detallados (en español e ingles) y siguiendo la estrategia recomendada por Haynes de búsqueda por "eslabones"
1) Los sistemas de información o nuevos libros sistemáticos,
2) fuentes de información secundaria o guías de práctica clínica bien realizadas.
UpToDate®
TRIPDATABASE
Guidelines
CMA INFOBASE Clinical Practice Guideline
Evidencia en la Práctica Ambulatoria
Scottish Intercollegiate Guidelines Network
3) Revisiones sistemáticas y meta-análisis
4)Búsqueda de artículos en bases Medline, Embase, Lilacs en forma completa y exhaustiva, siguiendo los criterios antes enunciados.
5) También se exploraron las listas de referencias de los estudios incluídos, y se consultaron expertos.
El periodo cubierto por la búsqueda fue de 10 años, en español e inglés.
Dos revisores, de forma independiente, seleccionaron, extractaron y evaluaron la calidad de los estudios. Se utilizó un método simple para la valoración de la calidad:
Estudios seleccionados:
1) Seeman 2006: Se trata de un trabajo que analiza dos estudios internacionales, que evaluaron el efecto del estroncio ranelato (2 g/día) sobre la osteoporosis primaria. Estos estudios eran fase III, randomizados, doble ciegos, y controlados: Spinal osteoporosis therapeutic intervention (SOTI) y Treatment of peripheral osteoporosis (TROPOS) seguidos durante 3 años11-13.
2) Reginster 2008: Se trata de un estudio randomizado, doble ciego, controlado que evaluó el efecto del ranelato de estroncio (2 gramos/día) sobre la osteoporosis primaria durante 5 años de seguimiento (continuación del estudio TROPOS)14.
Dado que ambos estudios comparten pacientes, ya que ambos incluyen pacientes del estudio TROPOS, no realizamos tratamiento estadístico (meta-análisis) a la presente revisión sistemática.
RESULTADOS
Número de pacientes estudiados:
Uno de los estudios incluyó 1488 pacientes (151 del SOTI y 1405 del TROPOS) todos mujeres de edad mayor o igual a 80 años (sobre 6740 pacientes totales) (Seeman 2006); el otro incluyó 1128 mujeres mayores de 74 años (sobre 5091 mujeres post-menopáusicas), en total 2616 pacientes.
Duración del tratamiento:
3 años (Seeman, 2006)11
5 años (Reginster 2008)14
Abandono:
Abandonaron el estudio 701 pacientes (47.1%) (Seeman, 2006)11
El dropout en 5 años fue del 47% (Reginster 2008)14
Análisis estadístico:
El análisis de sobrevida fue realizado mediante la curva de Kaplan-Meier.
Los grupos de tratamiento fueron comparados usando un modelo de Cox (Seeman, 2006)11
El análisis de sobrevida fue realizado mediante la curva de Kaplan-Meier.
Los grupos de tratamiento fueron comparados usando un modelo de Cox, y reconfirmado mediante el uso del log rank test (error tipo I del 5%)
Análisis de covariables: Student test y el número de pacientes con pérdida de talla: chi cuadrado (Reginster 2008)14.
Fracturas
Cuando se utilizaron 2 gramos/día de ranelato de estroncio el riesgo de fractura se redujo al año un 37% (p=0.012) y a los 3 años un 22% (p=0.040) (Seeman, 2006)11, mientras que en otro estudio el riesgo de fractura se redujo un 15%: riesgo relativo 0.85 (0.73-0.99) p=0.025 luego de 5 años de tratamiento (Reginster 2008)14 (Tabla 1)

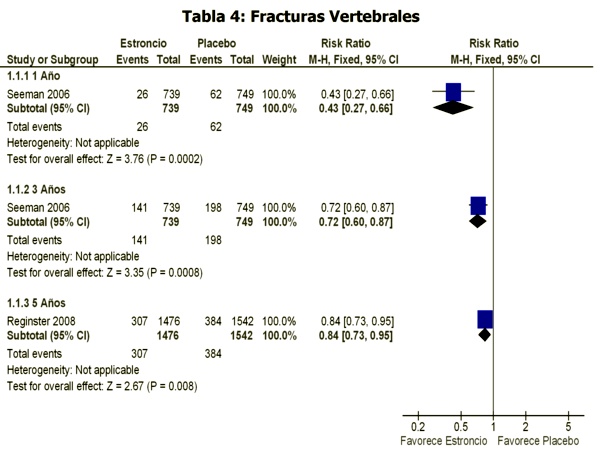
Fracturas vertebrales:
El riesgo de fractura vertebral se redujo al año un 59% (p=0.002), y a los 3 años un 32% (p<0.013) (Seeman, 2006)11, mientras que dicho riesgo se redujo un 24%: riesgo relativo 0.76 (0.65-0.88) p<0.001 tras 5 años de tratamiento (Reginster 2008)14 (Tablas 1 y 2)

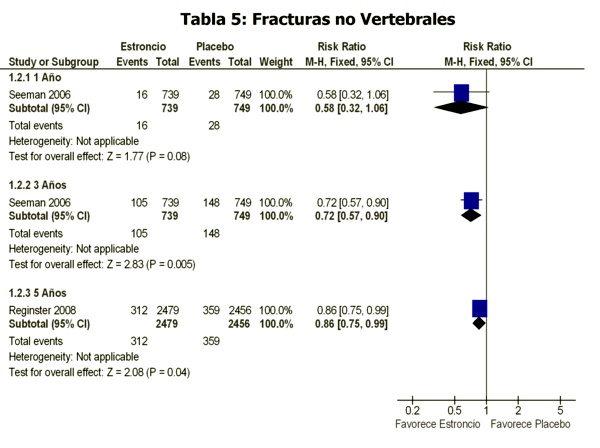
Fracturas no vertebrales:
El riego de fractura no vertebral e redujo al año un 41% (p=0.027), y a los 3 años un 31% (p<0.011), mientras que las fracturas no vertebrales mayores (cadera, muñeca, pelvis, sacro, clavícula, esternón y húmero) presentaron una reducción del 37% (p=0.003) (Seeman, 2006)11 (Tablas 1 y 3)
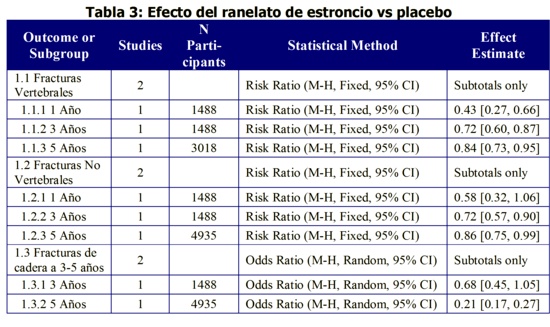
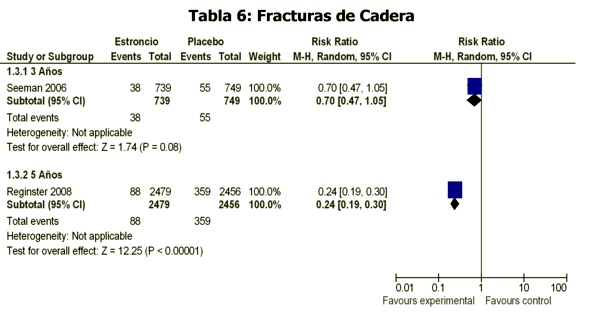
Fractura de Cadera:
El riego de fractura de cadera se redujo un 32%, pero sin alcanzar significación estadística (p=0.112) luego de 3 años de tratamiento con ranelato de estroncio (2 gr/día) (Seeman 2006)11, mientras que el riego de fractura de cadera se redujo un 43%: riesgo relativo 0.57 (0.33-0.97) p=0.036 luego de 5 años de igual tratamiento (Reginster 2008)14. (Tablas 1 y 4)
Eventos Adversos
El estroncio ranelato resultó ser bien tolerado, sólo reportándose en el grupo tratado con esta droga una mayor incidencia de nausea, diarrea, cefalea, hipertensión arterial (Seeman, 2006)11, así mismo este fármaco resultó ser también seguro en otro estudio, sólo reportándose en el grupo tratado con esta droga una mayor incidencia de nausea, diarrea, cefalea, dermatitis, eczema. La incidencia de tromboembolismo no resulto ser significativamente mayor en el grupo tratado (Reginster 2008)14.
DISCUSIÓN:
Dos ensayos cumplieron los criterios de inclusión: investigaron los efectos del ranelato de estroncio, en dosis de 2 gramos/día, comparado con placebo en una población mayor de 74 años de edad (muy anciana).
En base a los resultados pareciera haber una tendencia a un mayor efecto del tratamiento al año de su implementación (siempre teniendo en cuenta que los intervalos de confianza (IC) se solapan. La mayor reducción del riesgo de fractura se vio en aquellas vertebrales comparadas con las nos vertebrales (Tablas 4, 5 y 6). Así mismo, el mayor efecto anti-fractura se documento luego del año de tratamiento con ranelato de estroncio respecto de los 3 años del mismo, así como también se documento una mayor reducción del riesgo de fractura a los 3 años de tratamiento respecto de los 5 años del mismos (Tablas 4, 5 y 6). El primer fenómeno (mayor reducción del riesgo de fractura a nivel vertebral) podría deberse a un mayor efecto del ranelato de estroncio sobre la densidad mineral ósea vertebral versus la no-vertebral. Con respecto al segundo fenómeno (mayor reducción de riesgo al año de tratamiento que a los 5 años del mismo), éste podría explicarse por el hecho de verse cada vez más fortalecido el tejido óseo a mayor tiempo de exposición al efecto del estroncio.
A pesar la abundancia de datos a favor del tratamiento con estroncio, hay un riesgo relativo para fractura no vertebral al año de tratamiento que pasa por la unidad: 0.58 [0.32, 1.06]. En cuanto al riesgo de fractura a nivel de la cadera, existe ciertas diferencias respecto de los datos antes mencionados. Por un lado, la reducción del riesgo de fractura (32%) luego de 3 años de tratamiento con ranelato de estroncio documentada por el estudio Seeman 200611 no alcanzó significación estadística (p=0.112). Incluso el riesgo relativo pasa por la unidad: 0.68 [0.45, 1.05]
Sin embargo, el estudio Reginster 200814 demostró luego de 5 años de tratamiento con ranelato de estroncio una reducción mayor (43%) y estadísticamente significativa (p=0.036) (Tablas 3 y 6).
Estos datos podrían significar que tal vez el hueso de la cadera requiera un tiempo de exposición más prolongado al estroncio para verse beneficiado en una efectiva reducción de su riesgo de fractura. A la presente revisión sistemática no se le pudo realizar tratamiento estadístico (meta-análisis) debido a que los artículos en los que se basa compartían pacientes.
CONCLUSIÓN:
Hay pruebas que apoyan la utilidad del ranelato de estroncio, en dosis de 2 gramos diarios suministrado durante al menos 3 años, para reducir significativamente la incidencia de fracturas vertebrales y no vertebrales en mujeres muy ancianas con osteoporosis primaria.
REFERENCIAS:
-
1.- Boonen S, Mc Clung M, Eastell R, Fuleihan G, Barton I, Delmas P. Safety and efficacy of risedronate in reducing fracture risk in osteoporotic women aged 80 and older: implications for the use of antiresorptive agents in the old and oldest old. JAGS. 2004; 52: 1832-1839
2.- Consensus Development Conference: Diagnosis, Prophylaxis, and Treatment of Osteoporosis. In: American journal of medicine. Vol. Vol. 94, issue 3. 1993:561.
3.- NIH consensus development panel on osteoporosis prevention and diagnosis. Osteoporosis prevention, diagnosis, prophylaxis and treatment. Journal of american medical association 2001;285:785-95.
4.- Kiel D, Rosen C, Dempster D. Age-related bone loss. American society for bone and mineral research. 2008: 98-102
5.- Seeman E. Pathogenesis of bone fragility in women and men. Lancet 2002;359(9320):1841-50.
6.- WHO Study Group. Assessment of fracture risk and its application to screening for postmenopausal osteoporosis. Report of a WHO study group. World Health Organization technical report 1994; Vol. 843:1-129.
7.- Riggs BL, Parfitt AM. Drugs used to treat osteoporosis: The critical need for a uniform nomenclature based on their action on bone remodeling. Journal of bone and mineral research 2005;20(2):177-84.
8.- Sorbera LA, CastanËer J, Leeson PA, Bayes M. Strontium ranelate: Treatment and prevention of osteoporosis bone resorption inhibitor bone formation stimulant. Drugs of the future 2003;28(4):328-35.
9.- EMEA. PROTELOS. The committee for medicinal products for human use 2004.
10.- Ammann P, Shen V, Robin B, Mauras Y, Bonjour J, Rizzoli R. Strontium ranelate improves bone resistance by increasing bone mass and improving architecture in intact female rats. Journal of bone and mineral research. 2004; 19(12): 2012-2020
11.- Seeman E, Vellas B, Benhamou C, et. Strontium ranelate reduces the risk of vertebral and nonvertebral fracture in womwn eighty years of age and older. Journal of bone and mineral research. 2006.21; 7: 1113-1120
12.- Reginster J, Seeman E, De Verejoul M, Adami S, Compston J, Phenekos C, Devogelaer J, Diaz Curiel M, Sawicki A, Goemaere S, Sorensen O, Felsenberg D, Meunier P. Strontium ranelate reduces the risk of nonvertebral fractures in postmenopausal women with osteoporosis: treatment of peirpheral osteoporosis (TROPOS) study. The journal of clinical endocrinology & metabolism. 2005; 90(5): 2816-2822
13.- Meunier P, Roux C, Seeman E, Ortolani S, Badurski J, Spector T, Cannata J, Balogh A, Lemmel E, Pors-Nielsen S, Rizzoli R, Genant H, Reginster J. The New England Journal of Medicine. 2004; 350(5): 459-468
14.- Reginster J, Felsenberg D, Boonen S, et al. Effects of long-term strontium ranelate treatment on the risk of nonvertebral and vertebral fractures in postmenopausal osteoporosis. Arthritis & Rheumatism. 2008.58 (6):1687-1695.
