Indice del volumen Volume index
ComitÈ Editorial Editorial Board
ComitÈ CientÌfico Scientific Committee
- Menos de dos aÒos de evoluciÛn desde el diagnÛstico
- Ausencia de compromiso visceral
- Leucocitosis menor a 20000/mm3
- Presencia de 10 a 20% de cÈlulas de SÈzary circulantes
- Ausencia de adenopatÌas palpables
- Linfocitos T citotÛxicos cerca al rango normal (CD8 mayor 15%)
- Ausencia de quimioterapia intensiva previa
- Enfermedad en estadio placa que no comprometa m·s del 15% de la superficie corporal.
- Estadios eritrodÈrmicos IIIA o IIIB (pacientes con B0 o B1).
- Estadio IV A1 (paciente con B2) y con estadio T1, T2 o T4.
- Estadio IV A2 (pacientes con N3) y estadio T4.
FOTOF…RESIS EXTRACORP”REA EN LINFOMAS CUT¡NEOS DE C…LULAS T
Evelyn Andrea Zambrano MD, Paula Enz MD,
David De Luca MD,
Ricardo Galimberti MD.
Servicio de DermatologÌa, SecciÛn de Linfomas cut·neos, FotofÈresis y Fototerapia.
Hospital Italiano de Buenos Aires. Argentina
paula.enz @ hospitalitaliano.org.ar
Rev Electron Biomed / Electron J Biomed 2014;1:38-43.
Comentario de la revisora Dra. Anita Amalia Rossi. Servicio de DermatologÌa. Hospital del NiÒo de La Matanza. Provincia de Buenos Aires. Argentina
Comentario del revisor Dr. Carlos Adolfo FÈlix Musso. Ex-director del Hospital Municipal de MorÛn. Provincia de Buenos Aires. Argentina
RESUMEN:
Los linfomas cut·neos primarios son trastornos linfoproliferativos de cÈluas T, B o natural killer (NK), que comprometen la piel, sin evidencia de compromiso sistÈmico al momento del diagnÛstico.
Dentro del grupo de linfomas cut·neos primarios de cÈlulas T (LCCT), se encuentra a la micosis fungoide (MF) como la forma de presentaciÛn m·s frecuente y al sindrome de Sezary como una de las manifestaciones m·s agresivas.
El tratamiento se define teniendo en cuenta el estadio de la enfermedad y la condiciÛn clÌnica del paciente, siendo la FotofÈresis ExtracorpÛrea de primera elecciÛn en los estadios avanzados.
PALABRAS CLAVE: Fotoferesis extracorporea. Linfoma cutaneo. Enfermedad injerto contra huesped
SUMMARY:
Primary cutaneous lymphomas are lymphoproliferative disorders of T, B or natural killer (NK) cells, which involve the skin, with no evidence of systemic involvement at diagnosis moment.
Within the group of primary cutaneous T-cell lymphoma (CTCL), mycosis fungoides (MF) is the most common form of presentation and Sezary syndrome is one of the most aggressive manifestations.
Its treatment is defined by taking into account the stage of the disease and the patient's clinical condition, being the Extracorporeal Photopheresis the first therapeutic alternative in advanced stages.
KEY WORDS: Extracorporeal photopheresis. Cutaneous lymphoma. Graft versus host disease
INTRODUCCI”N
Los LCCT son trastornos linfoproliferativos de cÈlulas T, B o natural killer (NK), que afectan la piel sin existir evidencia de compromiso extracut·neo al momento del diagnÛstico.
Se presentan por lo general entre la cuarta y sexta dÈcada de la vida, ocupando el segundo lugar entre los linfomas no Hodgkin extranodales.
Dentro del grupo de de los LCCT, se destaca como forma de presentaciÛn m·s frecuente a la micosis fungoide (MF) en un 60% de los casos, manifest·ndose como una dermatosis de evoluciÛn lenta e indolente, encontrando tambiÈn formas de presentaciÛn agresivas con eritrodermia y fase leucÈmica como el sÌndrome de SÈzary, que constituye el 5% de los casos de LCCT1,2.
El diagnÛstico se realiza con base a la clÌnica, la histopatologÌa y la inmunohistoquÌmica, teniendo en cuenta tambiÈn el estudio del inmunogenotipo mediante tÈcnicas de biologÌa molecular por PCR.
La elecciÛn del tratamiento depende del estadio de la enfermedad y de la condiciÛn clÌnica del paciente, sin existir un tratamiento curativo para esta patologÌa. Teniendo en cuenta este concepto, hay varias opciones terapÈuticas, siendo la fotofÈresis extracorpÛrea de primera lÌnea en el sÌndrome SÈzary y de segunda lÌnea en casos micosis fungoide en estadios avanzados que no respondan a otros tratamientos.
La fotofÈresis extracorÛrea (FEC) o fotoquimioterapia extracorpÛrea es una terapia inmunomoduladora que combina la leucofÈresis con la fototerapia tradicional3.
En 1987 se presenta la primera publicaciÛn del uso de FEC en linfomas cut·neos4 y en 1988 fue aprobada por la FDA (Fud and Drug Administration) para el tratamiento de linfoma T cut·neo avanzado.
El tratamiento se realiza con un equipo que realiza un proceso en tres etapas: leucofÈresis, fotoactivaciÛn con 8-MOP (8-methoxypsoralen) y reinfusiÛn.
Durante la leucofÈresis se extrae sangre del paciente, la cual es sometida a centrifugaciÛn para obtener un concentrado de leucocitos, a este se le aplica la soluciÛn fotosensibilizante de 8MOP a una dosis entre 80 y 90ug, se expone a radiaciÛn ultravioleta A (UVA) a razÛn de 1 a 2 J/Cm2 y finalmente se reinfunde al paciente5. Este proceso tiene una duraciÛn aproximada de 3 a 4 horas.
El mecanismo de acciÛn de la FEC en los LCCT no est· totalmente claro, por un lado se plantea que induce apoptosis de linfocitos T por la incorporaciÛn del 8-MOP fotoactivado al ADN celular6, la cual ocurre aproximadamente 24 horas despuÈs del tratamiento; por otro lado se plantea un mecanismo inmunomodulador al favorecer la relaciÛn de los linfocitos Th1/Th27.
Se han descrito algunos factores que se consideran predictivos de buena respuesta al tratamiento con FEC8-9:
En los LCCT se realizan dos sesiones (1 ciclo) en dÌas continuos cada 2, 3 o 4 semanas, dependiendo compromiso de cada paciente; los ciclos se realizan durante 3 a 6 meses, momento en el cual se define la efectividad y continuidad del mismo.
Es un procedimiento bien tolerado y con mÌnimos efectos adversos, dentro de los cuales pueden aparecer febrÌcula, hipotensiÛn, y en el caso que el paciente tenga catÈter central, infecciones asociadas al mismo. Es importante destacar que durante el tratamiento con FEC la respuesta inmunolÛgica humoral y celular se mantiene normal.
Desde el primer estudio en 1987, se han realizado m˙ltiples publicaciones de FEC como monoterapia o en combinaciÛn con otras terapÈuticas para el tratamiento del linfoma cut·neo, con tazas de respuesta variables.
El tratamiento puede realizarse solo o combinado con inmunomoduladores. Estos est·n indicados en pacientes que no responden de manera satisfactoria a la monoterapia con FEC. En 1996 Gottlieb et al hicieron un estudio retrospectivo de 10 aÒos con pacientes que realizaron monoterapia con FEC vs. terapia combinada con interferÛn alfa, encontrando mejor respuesta en los pacientes que realizaron tratamiento combinado10. Otras alternativas para uso combinado son el bexarotene, el metotrexate, el acitretin, el baÒo de electrones y el PUVA, todos estos con respuestas variables.
En 2003 Suchin et al.10 describen 47 pacientes con linfomas cut·neos en estadios avanzados y sÌndrome SÈzary que realizaron 6 ciclos de FEC, algunos de estos con tratamiento combinado con interferÛn, ambos grupos presentaron porcentajes similares de respuesta y una sobrevida media de 74 meses en los pacientes que realizaron terapia combinada, frente a 66 que realizaron monoterapia, lo que no mostrÛ una diferencia estadÌsticamente significativa.
Child et al. en 2004 realizan un estudio comparativo de PUVA y FEC en tratamiento de MF placa estadio inicial IB, quienes adem·s presentaban clonalidad T en sangre perifÈrica, encontr·ndose mejor respuesta en cuanto al compromiso cut·neo con el PUVA que con la FEC, y ninguno de los dos tratamientos repercutiÛ en los hallazgos en sangre perifÈrica12.
A travÈs de los aÒos se ha ampliado el uso de FEC en LCCT, utiliz·ndose tambiÈn en estadios tempranos de micosis fungoide; Talpur R, Demierre MF et al, encontraron buena respuesta clÌnica y en la calidad de vida en pacientes en estadios tempranos (IA, IB y IIA) que realizaron FEC sola o en combinaciÛn con modificadores de la respuesta biolÛgica13.
En 2007 Miller et al. revisaron estudios de pacientes en fases tempranas de linfomas cut·neos, observando una tasa de respuesta muy variable (entre el 30 y 80%) en los que realizan monoterapia con FEC, teniendo en cuenta esto y que presenta pocos efectos adversos, podrÌa considerarse como una alternativa terapÈutica en estadios temprano, pero deben realizarse m·s estudios para definir su verdadera efectividad14. Se debe tener en cuenta que la indicaciÛn en estos casos a˙n es controvertida. En un estudio retrospectivo, Quaglino P, Knobler R et al describen 51 pacientes con linfomas cut·neos eritrodÈrmicos, de los cuales 39 tenÌan SS y 12 MF; 13 pacientes recibieron FEC como primera indicaciÛn terapÈutica despuÈs del diagnÛstico y en total 27 pacientes (57%) la recibieron como terapia ˙nica. Se obtuvo respuesta clÌnica en 32 de los 51 pacientes (63%), con 16% respuesta completa y 47% respuesta parcial15.
Siguiendo las ˙ltimas guÌas para el manejo de FEC en LCCT publicadas por Knobler et al2 en este aÒo, se considera como indicaciÛn de primera lÌnea en:
Los estadios descritos anteriormente teniendo en cuenta la revisiÛn de estadificaciÛn y clasificaciÛn de MF y SS seg˙n la Society for Cutaneous Lymphomas (ISCL) and the cut·neos lymphomas task force of the European Organization of Research and Treatment of Cancer (EORTC)16. Ver tabla 1 y 2.
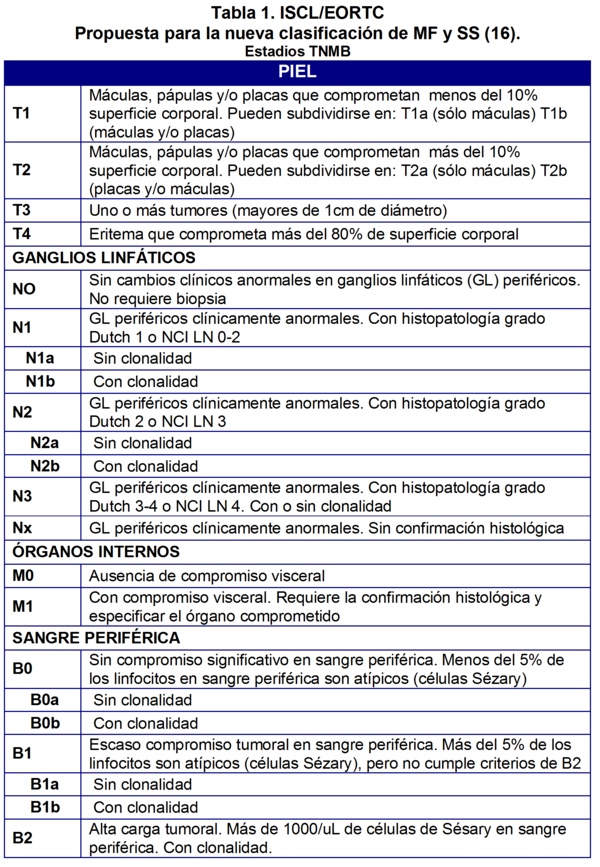
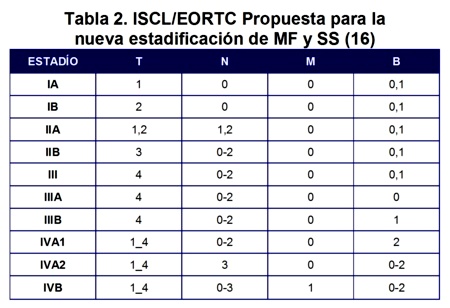
En conclusiÛn la FEC es una muy buena opciÛn terapÈutica, con buen nivel de tolerancia para pacientes con diagnÛstico de linfoma cut·neo de cÈlulas T en estadios avanzados o pacientes en estadios tempranos recalcitrantes al tratamiento ya sea como monoterapia o como terapia combinada
REFERENCIAS
1. Fung MA, Murphy MJ, Hoss DM, Grant-Kels JM. Practical evaluation and management of cutaneous lymphoma. J Am Acad Dermat 2002; 46: 325-60.
2. Knobler R et al. Guidelines on the use of extracorporeal photopheresis. J Eur Acad Dermatol Venereol 2014 Jan; 28: 1-37.
3. PÈrez Carmona L, Harto CastaÒo A, Diez Recio E, JaÈn Olasolo P. Actas Dermosifiliogr. 2009;100:459-71.
4. Edelson R, Berger C, Gasparro F, Jegasothy B, Heald P, Wintroub B, et al. Treatment of cutaneous T-cell lymphoma by extracorporeal photochemotherapy; preliminary results. N Engl J Med. 1987; 316: 297-303.
5. Knobler RM, Trautinger F, Graninger W, Macheiner W, Gruenwald C, Neumann R, et al. Parenteral administration 8-methoxypsoralen in photopheresis. J Am Acad Dermatol. 1993.
6. Rook AH, Suchin KR, Kao DMF, Yoo EK, Macey WH, DeNardo BJ, et al. Photopheresis: clinical applications and mechanism of action. J Invest Dermatol Symp Proc. 1999; 4:85-90.
7. Di Renzo M, Rubegni P, De Aloe G, Paulesu L, Pasqui AL, Andreassi L, et al. Extracorporeal photochemotherapy restores Th1/Th2 imbalance in patients whith earley stages cutaneous T-cell lymphoma. Immunology. 1997;92:99-103.
8. Scarisbrick JJ, Taylor P, Holtick U et al. UK Consensus statement on the use of extracoroporeal photopheresis for treatment of cutaneous T-cell lymphoma and chronic graft versus host disease. Br J Dermatol 2008; 158: 659-678.
9. Knobler R, Jantschitshc C. Extracorporeal photochemoimmunotherapy in cutaneous T-cell lymphoma. Transfus Apher Sci 2003; 28: 81-89.
10. Gottlieb SL, Wolfe JT, Fox FE, DeNardo BJ, et al. Treatment of cutaneous T cell lymphoma with extracorporeal photopheresis monotherapy and in combination with recombinant interferon alpha: a 10 year experience at a single institution. J Am Acad Dermatol. 1996; 35: 946-57.
11. Suchin KR, Cucchiara AJ, Gottleib SL et al. Treatment of cutaneous T cell lymphoma with combined immunomodulatory therapy: a 14 year experience at a single institution. Arc Dermatol 2002; 138: 1054-1060.
12. Child FJ, Mitchell TJ, Whittaker SJ, Scarisbrick JJ, et al. Randomized cross-over study to compare PUVA and extracorporeal photepheresis in the treatment of plaque stage (T2) mycosis fungoides. Clin Ex Dermatol. 2004; 29: 231-6.
13. Talpur R, Demierre MF, Geskin L, Baron E, Pugliese S et al. Multicenter photopheresis intervention trial in early stage mycosis fungoides. Clin Lymphoma Myeloma Leuk 2011 apr; 11 (2):219-27.
14. Miller JD, Kirkland EB, Santo Domingo D, Scull H, Jekutis B, Dallas M, et al. Review of extracorporeal photopheresis in early-stage (IA, IB and IIA) cutaneous T cell lymphoma. Photodermatol Photoimmunol Photomed. 2007; 23: 163-71.
15. Quaglino P, Knobler R, Fierro MT, et al. Extracorporeal photopheresis for the treatment of erytrhodermic cutaneos T cell lymphoma: a single center clinical experience with long-term follow-up data and a brief over view of the literature. Int J Dermatol 2013; 52: 1308-1318.
16. Olsen E, Vonderheid E, Pimpinelli N et al. Revisions to the staging and clssification of micosis fungoides and Sezary synfrome: a proposal of the International Society for Cutaneous Lymphomas (ISCL) and the cut·neos lymphomas task forcÈ of the European Organization of Research and Treatment of Cancer (EORTC). Blood 2007; 110: 1713-1722.
CORRESPONDENCIA:
Dra. Paula Enz.
SecciÛn de Linfomas cut·neos, FotofÈresis y Fototerapia. Servicio de DermatologÌa. Hospital Italiano de Buenos Aires.
Buenos Aires
Argentina
paula.enz @ hospitalitaliano.org.ar
