Indice del volumen Volume index
Comitť Editorial Editorial Board
Comitť CientŪfico Scientific Committee
LINFOMA DE C…LULAS DEL MANTO REFRACTARIO: TEMSIROLIMUS COMO OPCI”N DE TRATAMIENTO
Virginia Benito IbŠŮez1, Sara Barbadillo Villanueva1,
Beatriz Cuevas Ruiz2, MarŪa Paz Espinosa Pťrez1.
1Servicio de Farmacia, 2Servicio de HematologŪa.
Hospital Universitario de Burgos. Burgos, EspaŮa
vbenitoi @ saludcastillayleon.es
Rev Electron Biomed / Electron J Biomed 2015;3:9-14.
Comentario del revisor Prof. Francisco Abad, PhD, MD. Servicio de FarmacologŪa ClŪnica. Hospital de la Princesa. Madrid.
Comentario del revisor Prof. Sandro Bustamante. M.Sc. Programa de FarmacologŪa Molecular y ClŪnica. ICBM - Facultad de Medicina Universidad de Chile. Santiago de Chile. Chile.
RESUMEN
Introducciůn:Temsirolimus es un fŠrmaco indicado en linfoma de cťlulas del manto (LCM) en recidiva o refractariedad. La evoluciůn de este tipo de linfoma no Hodgkin (LNH) es agresiva y la respuesta al tratamiento es pobre.
Objetivos: Evaluar la efectividad y seguridad del temsirolimus en pacientes con LCM.
Material y mťtodos: Se realizů un estudio retrospectivo observacional en un hospital de tercer nivel de los pacientes en tratamiento con temsirolimus para la indicaciůn de LCM, desde noviembre del 2011 hasta abril del 2015.
Resultados: Se estudiaron cinco pacientes, todos varones tratados con temsirolimus con un rango de edad de 78 a 91aŮos. Se administrů el fŠrmaco en monoterapia en tres casos, y en los otros dos se asociů a rituximab.
El tratamiento se indiců desde 2 a 5 lŪnea. La mediana de supervivencia libre de progresiůn (SLP) fue de 1,1 meses (0,5-8) y la mediana de supervivencia global (SG) fue de 4,9 meses (0,5-10).
Con respecto a la tolerabilidad, los tres pacientes en monoterapia tuvieron reducciůn de dosis debido a acontecimientos adversos. Las reacciones mŠs frecuentes fueron anemia (100%) y neutropenia, trombocitopenia e infecciůn con un 60%.
Discusiůn: Las medianas de SLP y SG son menores que en el ensayo clŪnico del medicamento (4,8 meses y 12,8 meses respectivamente). Hay que tener en cuenta que nuestra muestra es pequeŮa de edad muy avanzada y que algunos pacientes tenŪan enfermedades asociadas graves.
Los efectos adversos observados son los esperados, manejables con reducciůn de dosis.
PALABRAS CLAVE: Linfoma no Hodgkin. Inhibidor de mTOR. Linfoma de alto grado. Tratamiento en recaŪda.
SUMMARY
Introduction: Temsirolimus is a drug approved for relapsed or refractory Mantle Cell Lymphoma (MCL). Disease progression of this Non-Hodgkin Lymphoma is aggressive and has a poor treatment response.
Objectives: To evaluate efficacy and safety on temsirolimus in MCL.
Materials and methods: A retrospective observational study was conducted in a third level hospital of the patients receiving temsirolimus as a MCL treatment, from November 2011 to April 2015.
Results: Five patients were studied, all male aged between 78 to 91 years. Three patients received the drug in monotherapy and two in combination with rituximab.
Line of treatment varied from second line to fifth line. Progression Free Survival (PFS) was 1,1 months (0,5-8) and Overall Survival (OS) was 4,9 months (0,5-10).
Concerning tolerability, the three patients in monotherapy had dose reductions due to adverse effects. Most frequent events of both monotherapy and combination treatment were anemia (100%) followed by neutropenia, thrombocytopenia and infection (all of them 60%).
Discussion: PFS and OS are smaller than in the clinical trial (4,8 months and 12,8 months respectively). It must be taken into account that our sample size is small, aged and with severe comorbilities.
Adverse effects observed are the spectated, all manageable with dose reductions.
Key words: Non-Hodgkin lymphoma. MTOR inhibitor. High-grade lymphoma. Relapse treatment
INTRODUCCI”N
El linfoma de cťlulas del manto (LCM) es un tipo de linfoma no Hodgkin (LNH) de linfocitos B que representa entre un 2.5-10% de todos los linfomas1. El comportamiento biolůgico es de carŠcter agresivo (clasificaciůn de la OMS 2008)2, con una supervivencia media de 2 a 3 aŮos presentŠndose en estadios avanzados hasta en el 70% de los casos. El diagnůstico es mayoritario en individuos de edad avanzada, con una media de 68 aŮos y predominantemente en varones, proporciůn 4:1 con respecto a las mujeres 3.
En pacientes en recaŪda o refractarios las expectativas de vida son cortas.
FenotŪpicamente se caracteriza por la presencia de una poblaciůn monoclonal de lŪnea B CD5+ y sobreexpresiůn de ciclina D1 asociada a la presencia de la translocaciůn t(11;14)1.
La sintomatologŪa que presentan estos pacientes suele ser de astenia, apariciůn de adenopatŪas y enfermedad diseminada que puede afectar a mťdula ůsea, bazo, hŪgado y tracto digestivo1,3. Cuando se invade la mťdula ůsea y sangre perifťrica hablamos de leucemizaciůn y ocurre en el 35% de los casos, el pronůstico es inferior en estos casos4.
Se ha elaborado un Ūndice pronůstico (MIPI) con los siguientes factores: edad, estado general (ECOG), niveles de lactato deshidrogenasa (LDH) y cifra de leucocitos que clasifica a los pacientes en 3 grupos de riesgo pronůstico 5-6.
Una pequeŮa proporciůn de los pacientes cursan con una enfermedad indolente, por lo que en estos casos se puede adoptar una actitud de "esperar y ver"7. Sin embargo, como ya se ha dicho anteriormente, la mayorŪa de los diagnůsticos se realizan en estadios avanzados, siendo ya una entidad mayoritariamente incurable, que requiere tratamiento inmediato. Aunque el LCM es un linfoma quimiosensible y radiosensible, se caracteriza por tener unas respuestas de corta duraciůn8.
Teniendo en cuenta la edad de los pacientes al diagnůstico, se plantea la realizaciůn de trasplante de mťdula ůsea previo tratamiento con esquemas de inducciůn que incluyan altas dosis de ARA-C en pacientes jůvenes. Aquellos que no sean candidatos a trasplante se pueden considerar diferentes esquemas de quimioterapia como R-CHOP [rituximab, ciclofosfamida, doxorrubicina, vincristina, prednisona], Rituximab-Bendamustina, Bortezomib, Temsirolimus, Talidomida9.
En pacientes en recaŪda o refractarios en los cuales las expectativas de vida son cortas, una de las opciones de tratamiento que encontramos es temsirolimus, un inhibidor selectivo mTOR (diana de la rapamicina en las cťlulas de mamŪfero). Con la uniůn a mTOR se consigue retrasar el crecimiento en la fase G1 del ciclo celular y la interrupciůn en la traducciůn de algunas proteŪnas reguladoras como las ciclinas de tipo D. AdemŠs podrŪa tener la capacidad tambiťn de deprimir niveles de factores inducibles por la hipoxia (HIF) y factor de crecimiento del endotelio vascular (VEGF) reduciendo asŪ la angiogťnesis del tumor10.
AdemŠs se puede asociar al temsirolimus el anticuerpo rituximab, la combinaciůn de ambos demostrů mejores resultados frente a la monoterapia en respuestas globales, respuestas completas y supervivencia libre de enfermedad 11.
MATERIAL Y M…TODOS
Se realizů un estudio retrospectivo observacional en un hospital de tercer nivel de los pacientes que se trataron con temsirolimus para la indicaciůn de LCM, desde noviembre del 2011 hasta abril del 2015.
Los datos se obtuvieron de la historia clŪnica de los pacientes y del programa informŠtico de dispensaciůn a pacientes ambulantes.
Los datos recogidos fueron: edad, sexo, enfermedades asociadas, estadio de la enfermedad (clasificaciůn Ann-Arbor)12, Ūndice pronůstico de LCM (MIPI), lŪneas de tratamiento previas, dosificaciůn y reacciones adversas asociadas a temsirolimus, supervivencia libre de progresiůn (SLP) y supervivencia global (SG).
RESULTADOS
Un total de cinco pacientes se trataron con temsirolimus en las fechas seleccionadas. Todos fueron hombres con edades comprendidas entre los 78-91aŮos. El estadio de la enfermedad al diagnůstico segķn la clasificaciůn Ann-Arbor fue de grado I en un paciente (afectaciůn de una ķnica regiůn ganglionar o de un ķnico sitio u ůrgano extraganglionar) y de grado IV en el resto (afectaciůn diseminada de uno o mŠs ůrganos extralinfŠticos asociada o no con enfermedad ganglionar).
En cuanto al pronůstico calculado para nuestros pacientes segķn MIPI un paciente correspondŪa al grupo de bajo riesgo, dos al de riesgo intermedio-alto y dos al de riesgo alto.
Es importante destacar que en cuatro de los casos se encontraron comorbilidades graves: un paciente con cŠncer hepŠtico, otro con hipertensiůn pulmonar, otro con isquemia coronaria crůnica y otro con insuficiencia renal crůnica en hemodiŠlisis.
Como se puede ver tambiťn en la Tabla 1, se eligiů la monoterapia en tres pacientes: dos iniciaron el tratamiento segķn las indicaciones, con dosis de 175 mg una vez a la semana durante 3 semanas, para seguir despuťs con 75 mg semanales, sin embargo ambos dos precisaron reducciones de dosis debido a reacciones adversas, continuŠndose el tratamiento al 80% de la dosis en uno de los casos por astenia intensa, y al 60% en el otro por anemia. El tercer paciente de monoterapia que fue diagnosticado de LCM leucemizado, iniciů temsirolimus a dosis bajas (50 mg) desde el primer ciclo por su mal estado general. Tambiťn requiriů reducciůn de dosis (25mg) por trombopenia.
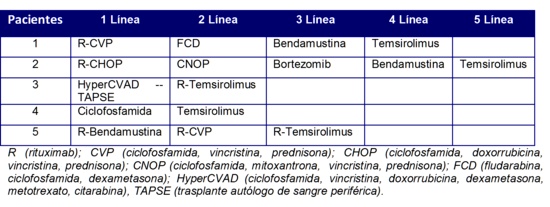
Tabla 1: Datos pacientes
En los dos pacientes restantes se optů por un tratamiento combinado con rituximab (a dosis de 375 mg/m2) semanalmente durante el primer mes, con una dosis de temsirolimus de 25 mg tambiťn semanal.
El tratamiento se indiců desde 2 a 5 lŪnea. (Tabla 2)
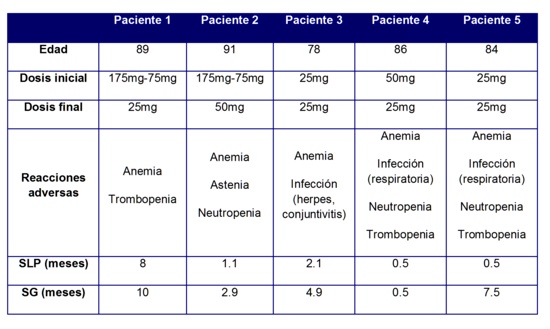
Tabla 2: LŪneas previas de tratamiento de los pacientes
La mediana de SLP fue de 1,1 meses (0,5-8) y la mediana de SG fue de 4,9 meses (0,5-10). Desde el momento del diagnůstico la mediana de supervivencia fue de 5 aŮos4-6.
La reacciůn adversa mŠs frecuente fue la anemia dŠndose en el 100% de los casos. Fue controlada con transfusiones sanguŪneas y precisů de reducciůn de dosis en un paciente. Neutropenia, trombocitopenia e infecciůn fueron los efectos secundarios de mayor incidencia con un 60% cada uno.
DISCUSI”N
Las medianas de SLP y SG son menores que en el ensayo clŪnico pivotal del medicamento (4,8 meses y 12,8 meses respectivamente). Sin embargo contamos con una muestra muy pequeŮa de edad avanzada y con pacientes que cuentan con comorbilidades graves que pueden modificar la supervivencia.
Los estudios publicados demuestran mejores resultados con la asociaciůn de rituximab. Pese a nuestro tamaŮo muestral insuficiente, nuestros datos no sugieren esto.
Los efectos adversos mŠs frecuentes son los observados en los ensayos realizados, con frecuencias mayores a las medianas, pero esperables en el rango de edad avanzada (> 65 aŮos).
En el momento que se escriben estas lŪneas se encuentra disponible el fŠrmaco inhibidor de la tirosin kinasa de bruton ibrutinib. En el estudio de fase III se compara con placebo en linfoma de cťlulas del manto en 111 pacientes refractarios o en recaŪda, el 21% de los pacientes alcanzů una respuesta completa y el 47% tuvo una respuesta parcial. La duraciůn media de la respuesta al tratamiento fue de 17,5 meses. Esta podrŪa ser una opciůn para futuros pacientes en recaŪda13-14.
REFERENCIAS
1. Jaffe ES, Harris NL, Vardiman JW, Campo E, Arber DA. Hematopathology 2011, Chapter 21, 333-348.e5
2. Jaffe ES, Harris NL, Stein H, Isaacson PG. Classification of lymphoid neoplasms: the microscope as a tool for disease discovery. Blood. 2008; 112(12):4384-99
3. Hoffman R, Benz E, Silberstein L, Heslop H, Weitz J, Anastasi J. Hematology: Basic Principles and Practice, sixth edition 2013. Chapter 80, 1226-1235.e3
4. Fabregat AB,Estela PL, Valero M. Leucemizaciůn de linfoma de cťlulas del manto. Revista del Laboratorio ClŪnico, December 2015
5. Hoster E, Dreyling M, Klapper W, Gisselbrecht C, van Hoof A, Kluin-Nelemans HC, et al. A new prognostic index (MIPI) for patients with advanced-stage mantle cell lymphoma. Blood. 2008;111:558-65.
6. MIPI: Mantle Cell Lymphoma International Prognostic Index. Disponible en: http://www.european-mcl.net/en/clinical_mipi.php
7. Sociedad Castellano-Leonesa de HematologŪa y Hemoterapia. GuŪas Linfoma 2014. 30,31p.
8. GarcŪa-Noblejas A, Cannata J, Arranz R. Actualizaciůn del tratamiento del linfoma de cťlulas del manto 2011
9. Campo E, Rule S. Mantle cell lymphoma: evolving management strategies. January 1, 2015; Blood: 125 (1)
10. Ficha tťcnica Torisel EMEA. Consultada el 12/12/2015.
11. Navarro B, GarcŪa-Marco JA. Linfoma de cťlulas del manto: Ņhacia una estrategia terapťutica individualizada? Medicina ClŪnica, 2015-06-22, Volumen 144, Nķmero 12, Pages 553-559
12. Armitage J. Staging Non-Hodgkin Lymphoma. CA Cancer J Clin 2005;55:368-376.
13. Ficha tťcnica de Imbruvica®. AEMPS. Consultada el 15/12/15
14. Bernard S et al. Activity of ibrutinib in mantle cell lymphoma patients with central nervous system relapse. October 1, 2015; Blood: 126 (14)
CORRESPONDENCIA:
Virginia Benito IbŠŮez.
Servicio de Farmacia
Hospital Universitario de Burgos
09006 Burgos
vbenitoi @ saludcastillayleon.es
Comentario del revisor Prof. Francisco Abad, PhD, MD. Servicio de FarmacologŪa ClŪnica. Hospital de la Princesa. Madrid.
Los pacientes con linfoma de cťlulas del manto presentan un pronůstico muy malo por lo que suelen probar diferentes tratamientos.
El temsirolimus es una de las alternativas mŠs recientes. Este estudio demuestra que el efecto beneficioso de los fŠrmacos en la prŠctica clŪnica diaria (efectividad) es muy inferior a la observada en los ensayos clŪnicos (eficacia), lo que se explica porque los pacientes incluidos en los ensayos clŪnicos son una muestra muy seleccionada que no presentan la gravedad ni las enfermedades concomitantes que se presentan en el mundo real.
Comentario del revisor Prof. Sandro Bustamante. M.Sc. Programa de FarmacologŪa Molecular y ClŪnica. ICBM - Facultad de Medicina Universidad de Chile. Santiago de Chile. Chile.
Aborda la temica esperable a juzgar por el tulo del trabajo, aunque el foco estŠ enfatizado en la patologŪa del linfoma que en temsirolimus.
Si bien la revisiůn bibliogrŠfica no considera la informaciůn del estado del arte en la materia1, los resultados son relativamente claros y las tablas estŠn bien elaboradas, son comprensibles y aportan informaciůn al lector.
1Hess et al. Effect of prognostic classification on temsirolimus efficacy and safety in patients with relapsed or refractory mantle cell lymphoma: a retrospective analysis. Exp Hematol Oncol 2015;4:11.
