Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
- Personas menores de 18 o mayores de 70 ańos.
- Mujeres embarazadas.
- Pacientes con desnutrición (IMC>19) o con obesidad (IMC> 35)
- Pacientes amputados.
- Retención hidrosalina grave (cirrosis, ICC, hipotiroidismo avanzado)
- Pacientes hospitalizados con inestabilidad hemodinámica.
- Estudios de potenciales donantes de rińón.
- Prerrenal (hipoperfusión renal)
- Renal intrínseca glomerular
- tubular
- intersticial
- vascular
- Postrrenal (obstrucción urinaria)
- Pacientes ańosos
- Raza negra o etnia latina, asiática
- Genéticos
- Bajo peso al nacer
- Hipertensión arterial
- Diabetes
- Enfermedad cardiovascular
- Albuminuria/proteinuria
- Obesidad
- Síndrome metabólico
- Dislipemia
- Hiperuricemia
- Tabaquismo
- Bajo nivel socioeconómico
- Nefrotóxico (AINEs, hierbas, plomo)
- Sobrecarga de volumen con expansión del compartimiento extracelular
- Hipercalemia
- Acidosis metabólica
- Hipertensión arterial
- Anemia
- Alteraciones del metabolismo fosfocálcico
- Anorexia
- Náuseas y vómitos
- Pericarditis aguda
- Neuropatía periférica
- Alteraciones del SNC caracterizadas por disminución de la concentración, letargia, convulsiones y coma
- Dosaje de Hb, recuento de glóbulos rojos y hematocrito
- Parámetros hematimétricos (volumen corpuscular medio), hemoglobina corpuscular media)
- Perfil de Fe:
- Ferritina
- Ferremia y capacidad total de transporte de hierro (TIBC).
- TSAT (que evalúa la disponibilidad de Fe)
- Agrava el hiperparatiroidismo secundario
- Incrementa el catabolismo muscular
- Altera la contractilidad miocárdica y lleva a insuficiencia cardíaca
- Aumenta la reabsorción ósea/osteopenia
- Resistencia a la hormona de crecimiento e insulina
- Agota los sistemas buffers sistémicos
- Desarrolla inflamación sistémica
- Tendencia a la hipotensión arterial
- Hipertensión arterial
- Tabaquismo
- Diabetes
- Dislipemia
- Edad avanzada
- Toxinas urémicas
- Anemia
- Ciertas citoquinas
- Aumento de la carga de calcio
- Alteraciones del metabolismo mineral y óseo
- Estado inflamatorio
- evitar agentes de osmolaridad alta.
- medios de contraste no iónicos.
- utilizar la mínima dosis posible del radiocontraste.
- suspender previamente los fármacos potencialmente nefrotóxicos, particularmente metformina.
- hidratación adecuada con solución salina 0.9% 12hs antes, durante y después del procedimiento.
- monitoriar el FG 48-96 horas después del estudio.
- No se ha incluido como recomendación en las guías KDIGO el uso de N-acetilcisteína o ácido ascórbico como profilaxis de la nefropatía por contrastes. Otras guías recomiendan N- acetilcisteína 600 mg VO 12 hs. antes del estudio contrastado, 600 mg coincidiendo con el estudio y 600 mg posteriores.
- HTA refractaria > 150/90 mmHg a pesar de la combinación de 3 drogas de clases complementarias.
- Proteinuria > 0.5-1 g/día.
- Proteinuria progresiva y/o hematuria persistente.
- Diabetes con incremento de la proteinuria.
- Hematuria macroscópica sin causa urológica.
- Edema pulmonar recurrente con sospecha de estenosis de arteria renal.
- Caída de TFG (> 30% en 4 meses) sin explicación aparente o con sospecha de estenosis de arteria renal.
- Anemia inexplicada (<10 g/dL) en estadios 1-3.
- PTH > 70 ng/mL sin déficit de Vit. D
- Casos con sospecha de causa genética o rara de ERC.
LA ENFERMEDAD RENAL CRONICA: SUS ASPECTOS CLÍNICOS Y SU ABORDAJE DIAGNÓSTICO Y TERAPÉUTICO.
Gabriela A. Gonzalez, Miguel A. Nadal
División Nefrología Hospital de Clínicas Jose de San Martín.
Universidad de Buenos Aires.
Buenos Aires. Argentina
gagonzalez @ intramed.net
Rev Electron Biomed / Electron J Biomed 2017;1:30-50.
Comentario del revisor Dra. Mariana Ciocchini. Instituto Daomi - Buenos Aires, Argentina
Comentario de la revisora Susana Gabriela Pérez MD. Especialista en Nefrología. Posgrado de Efectividad Clínica, Analista de Datos Médicos en Diaverum. Argentina.
RESUMEN
El el presente artículo se realiza una detallada revisión respecto de cómo se diagnostica la enfermedad renal crónica, cuáles son sus principales causas y características clínicas, cuáles sus complicaciones clínicas y su abordaje terapéutico según el estado actual del conocimiento.
PALABRAS CLAVE: Enfermedad renal crónica. Definición. Diagnóstico. Tratamiento.
SUMMARY: STROMAL AND TROPHOBLASTIC LESIONS IN PLACENTAL VILLI OF PREGNANT WITH ANTIPHOSPHOLIPID SYNDROME IN ANTITHROMBOTIC THERAPY.
In the present article a detailed review is made regarding how chronic kidney disease is diagnosed, its main causes and clinical characteristics, its clinical complications and its therapeutic approach according to the current state of knowledge.
KEY WORDS: Chronic kidney disease. Definition. Diagnosis. Treatment.
INTRODUCCIÓN
ENFERMEDAD RENAL CRONICA
La enfermedad renal crónica1 (ERC) es un grupo heterogéneo de entidades caracterizadas por alteraciones en la estructura de los rińones, con tendencia al deterioro progresivo de la función renal que se manifiesta en forma variada dependiendo de la causa subyacente y severidad de la enfermedad.
El término de ERC terminal alude al estadio de la enfermedad de base que requiere diálisis o trasplante renal .
Una injuria inicial a los rińones puede conducir a la ERC a través de una variedad de manifestaciones clínicas desde la hematuria asintomática, proteinuria de magnitud variable, hipertensión arterial y diferentes grados de insuficiencia renal.
Muchos pacientes se recuperan y otros mantienen signos de enfermedad renal, que pueden progresar a estadio terminal. Además, hay variaciones de la actividad en cada una de las nefropatías que explican la diferente respuesta individual a la injuria.
ADAPTACION FUNCIONAL
El rińón es capaz de adaptarse al dańo inicial aumentando la filtración glomerular en las nefronas normales remanentes, proceso denominado hiperfiltración adaptativa, que explica porque algunos pacientes con nefropatías leves presentan creatinina normal o casi normal. También otros mecanismos compensatorios como los tubulares permiten que las concentraciones del sodio, potasio, calcio, fósforo y contenido corporal total del agua, permanezcan dentro del rango normal2.
HIPERFILTRACION
En los pacientes en quienes inicialmente la adaptación de la hiperfiltración impresionó como beneficiosa, es importante saber que posteriormente resulta en un dańo a largo plazo de los glomérulos remanentes que terminan clinicamente con proteinuria e insuficiencia renal progresiva debido a esclerosis glomerular1,2.
No todos los pacientes tienen pérdida progresiva de la función renal. Algunos estudios muestran alto índice de progresión de algunas nefropatías y en otras un curso relativamente estable. La progresión está determinada por el tipo de enfermedad de base, ausencia o presencia de morbilidades como diabetes, hipertensión arterial, tabaquismo, obesidad, dislipemia, determinantes genéticos, raza, entre otros factores, en general coincidiendo con creatininas mayor a 1,5 mg/dl. La hiperfiltración de la nefrona remanente puede atenuarse con dieta hipoproteica por constricción de la arteriola aferente y por la administración de enalapril, que al inhibir a la enzima que convierte la angiotensina I en II, que fisiológicamente contrae la arteriola eferente, su dilatación por acción de esta droga, conducirá a disminuir la presión glomerular o hiperfiltración2.
La combinación de disminución del FG con proteinuria se asocia con un significativo aumento del riesgo de progresión. En cada uno de los niveles de FG, el aumento de la albuminuria confiere un mayor riesgo de eventos adversos2.
DEFINICION DE ENFERMEDAD RENAL CRONICA
La enfermedad renal crónica (ERC) se define como las anormalidades de la estructura renal o función, presentes por más de 3 meses, con implicancias sobre la salud1.
Se clasifica de acuerdo a las causas, categoría del filtrado glomerular (FG), y categoría de la albuminuria.
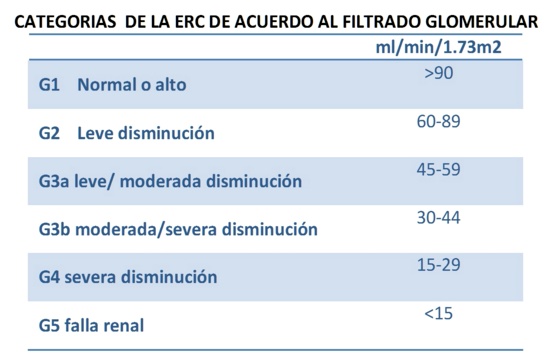

El grado de ERC que amerita estudios complementarios para diagnosticar con más precisión la nefropatía subyacente lo determina la presencia de albuminuria mayor de 30mg/24hs y el FG menor de 60 ml/min/1,73 m2 persistentes más de 3 meses, combinación que se asocia con elevada morbi mortalidad cardiovascular.
żCÓMO ESTIMAMOS EL FG?
Filtrado glomerular estimado (FGe): la evaluación del FG se llevará a cabo mediante la determinación de la creatinina sérica y una fórmula para estimar el FG ).
Las nuevas guías recomiendan el cambio de la ecuación para estimar el FG a la fórmula CKD-EPI (CKD Epidemiology Collaboration) de 20093.
Ecuación CKD-EPI2-3
Mujeres
Creatinina < 0,7 mg/dl FGe = 144 x (creatinina/0,7)-0,329 x (0,993)edad [x 1.159 r.negra]
Creatinina > 0,7 mg/dl FGe = 144 x (creatinina/0,7)-1,209 x (0,993)edad [x1.159 r.negra]
Varones
Creatinina < 0,9 mg/dl FGe = 141 x (creatinina/0,9)-0.411 x (0,993)edad [x1.159 r.negra]
Creatinina > 0,9 mg/dl FGe = 141 x (creatinina/0,9)-1,209 x (0,993)edad [x1.159 r.negra]
Ecuación MDRD-IDMS2-3
FGe = 175 x (creatinina)-1,154 x (edad)-0,203 x 0,742 (si mujer) x 1,21 (si etnia negra) L
a ecuación CKD-EPI, proporciona ventajas adicionales respecto al MDRD- IDMS, dado que presenta una mayor exactitud y mejora la capacidad predictiva del FG (especialmente entre valores de 60 y 90 ml/min/1,73 mm2) así como la predicción de mortalidad global y cardiovascular o del riesgo de presentar ERC avanzada.
Las nuevas guías KDIGO 2012 sugieren la medida de cistatina C en adultos con FG entre 45 y 59 ml/min/1,73 m2, sin otros marcadores de lesión renal, si se requiere una confirmación diagnóstica de ERC. Se debería usar entonces la ecuación CKD-EPI para cistatina C recientemente publicada.
Ecuación 2012 CKD-EPI cistatina C3:
133 x min (SCysC/0.8, 1) -0.499 x max (SCysC/0.8, 1) -1.328 x 0.996edad [x0.932 mujer].
SCysC: Cistatina C sérica (en mg/l), min indica el mínimo de SCysC/0.8 o 1, y max indica el máximo de SCysC/0.8 o 1.
Estas fórmulas NO deben ser usadas en m1-3:
LA EVALUACION DE UN PACIENTE CON CREATININA ELEVADA DE CUALQUIER DURACION INCLUYE4:
-
1. Historia clínica cuidadosa con examen físico completo
2. Antecedentes de creatininemias anteriores
3. Investigar la función renal actual con clearance de creatinina medido
4. Determinar la proteinuria de 24hs, con estudio cualitativo de la misma (uroproteinograma)
5. Sedimento urinario
6. Imágenes del rińón
7. Determinaciones serológicas para investigar enfermedades de sistema
8. Biopsia renal si los estudios no invasivos son insuficientes para un diagnóstico adecuado
IMPORTANCIA DEL ESTUDIO DE LA ORINA EN EL DIAGNOSTICO DE LAS NEFROPATIAS CRONICAS1-4
El examen de la orina brinda extensa información sobre las distintas estructuras del glomérulo y túbulo.
La incapacidad de concentrar la orina, característica de la ERC es un elemento a tener en cuenta. En las tubulopatías crónicas es característico el pH urinario alcalino en ayunas, como también con dieta rica en frutas y verduras.
La excreción de proteínas puede ser leve o severa, tubular o glomerular, dependiendo de la enfermedad de base.
El sedimento urinario de las nefropatías crónicas suele ser lo que comúnmente llamamos "blando" con escaso contenido celular, fundamentalmente en los pacientes cardiorrenales, con HTA o DBT.
Si la causa de la ERC fue una enfermedad glomerular pueden verse cilindros granulosos, hemáticos, céreos, anchos o leucocitarios en las nefritis tubulo intersticiales crónicas.
Los cilindros céreos y anchos son frecuentes de encontrar en glomerulopatías avanzadas.
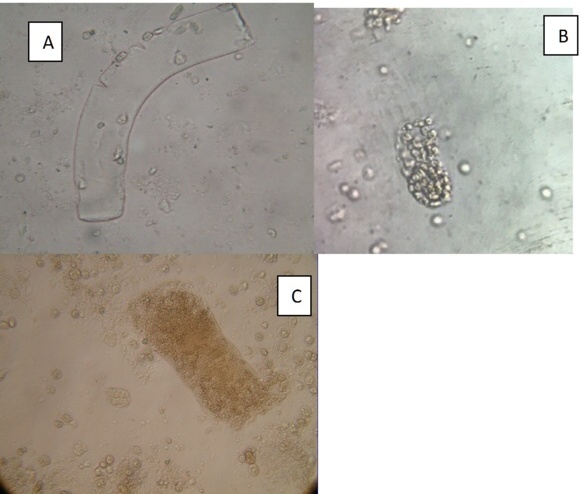
Fig A: cilindro céreo, B leucocitario, C hemático y ancho
CAUSAS DE NEFROPATÍAS CON INSUFICIENCIA RENAL
La siguiente clasificación de insuficiencia renal es clásica pero tiene vigencia clínica.
Las condiciones con hipoperfusión renal (hipovolemia efectiva) se encuentran en la insuficiencia cardíaca aguda o crónica y en la cirrosis hepática con hipertensión portal y se caracterizan por hiperazoemia con creatininas poco elevadas (llamativa disociación entre urea y creatinina plasmáticas), sodio urinario bajo, ausencia de proteinuria y sedimento urinario sin valor patológico.
Las glomerulopatías crónicas (con algún grado de insuficiencia renal) pueden expresarse con rasgos nefríticos como microhematuria dismórfica con acantocituria y cilindruria, en especial el cilindro hemático, y proteinuria de grado variable. Otras, con síndrome nefrótico, con o sin microhematuria y con cilindros grasos, cuerpos ovales grasos y lipiduria.
La tubulopatías agudas más comunes son la necrosis tubular aguda que complican situaciones de isquemia renal (hipoperfusión renal brusca, intensa y sostenida) o por causas tóxicas, generalmente secundarias a drogas como AINEs, antibióticos, etc. La orina de estos pacientes tiene proteinuria leve, sedimento urinario con abundantes cilindros granulosos oscuros y tubulares.
Las nefropatías intersticiales son varias como la poliquistosis renal, síndrome de Sjögren, nefrocalcinosis en contexto de hipercalcemias, sarcoidosis, nefropatía por reflujo y nefritis intersticiales agudas y crónicas y enfermedad quística medular.
Las vasculopatías más frecuentes son la nefroesclerosis hipertensiva que culmina afectando a glomérulos e intersticio. La estenosis de la arteria renal por ateroesclerosis o por las diferentes formas de displasia fibromuscular, pueden crónicamente terminar en la nefropatía isquémica. Por último, las microangiopatías trombóticas ocurren en diferentes entidades con anemia hemolítica microangiopática que deben siempre considerarse.
La nefropatía obstructiva aparece en agrandamiento benigno o maligno de la próstata, carcinoma de la vejiga o del trígono, y en la fibrosis retroperitoneal en sus diferentes etiologías.
IDENTIFICAR LA CAUSA DE LA ENFERMEDAD RENAL CRONICA5
Es esencial identificar la causa de la ERC como diabetes, uso de drogas nefrotóxicas como plomo, AINEs, enfermedades autoinmunes (LES), obstrucción urinaria, para así detener o enlentecer tanto la progresión como el riesgo de complicaciones.
La ERC se puede presentar en cualquiera de las condiciones que potencialmente desarrollan disfunción renal, siendo la nefropatía diabética la causa más frecuente de nefropatía terminal, seguida de la nefroesclerosis hipertensiva y de otras glomerulopatías primarias o secundarias.
ESTIMACION DE LA DURACION DE UNA NEFROPATIA
Establecer la duración de una nefropatía es un importante aspecto de la evaluación. Esto requiere de disponer de datos anteriores que muestren evidencia de compromiso renal como albuminuria/proteinuria, hematuria, aumento de la urea y/o creatinina plasmática, hipertensión arterial, nicturia o algún grado de anemia. El conocer la duración de la enfermedad estrecha las posibilidades del diagnóstico diferencial6-9.
VELOCIDAD DE DESARROLLO DE LA INSUFICIENCIA RENAL 6-8
Si bien la distinción entre injuria renal aguda (IRA), insuficiencia renal de rápida progresión e insuficiencia renal crónica es arbitraria, los siguientes criterios internacionalmente establecidos, ayudan a encasillar a esas categorías que tienen diferencias en la velocidad de afectación de la función renal.
La IRA se la define por el aumento de la creatinina comprobado en horas o días, de más de 0,3mg/dl en relación a una creatinina basal dentro de las 48hs o un incremento de 1.5 veces de un valor basal a los 7 días. La reducción de la diuresis < 3 mL/Kg durante 6 hs, es un criterio adicional que ayuda en el diagnóstico, como la aparición de proteinuria y un sedimento urinario anormal.
El grupo conocido como de injuria renal subaguda o de rápida progresión alude a la disminución de la función renal con el obligado incremento en la creatinina en un período menor a 3 meses. Como se comprende, en determinados pacientes existe algún grado de superposición entre este grupo y el anterior.
La ERC ya ha sido definida como el estado renal de un paciente con un Ccr < 60mL/min/1,73m2, albuminuria o alteraciones en las imágenes del rińón, con más de 3 meses de duración, con implicancias importantes para la salud.
Como se ha dicho, la duración o velocidad del deterioro de la función renal puede estimarse cuando se comparan creatininas y análisis de orina recientes con otros anteriores. En casos de no disponer de esta información, otros elementos de la historia clínica y del examen físico suelen aportar datos que orienten en la antigüedad de la nefropatía.
DATOS QUE ORIENTAN A LA ANTIGÜEDAD DE LA NEFROPATIA 6-9
-
a) cambios en el color de la orina como hematuria, indican proceso reciente.
b) aparición de edema/anasarca, enfermedad reciente.
c) creatinina basal con rápidos incrementos, orientan a proceso agudo.
d) creatinina elevada con niveles similares en los controles, apuntan a enfermedad crónica.
e) oliguria < 500mL/24hs compatibles con IRA, ya que las enfermedades crónicas evolucionan sin oligoanuria, y probablemente con nicturia expresión de poliuria.
f) tamańos renales reducidos indican entidades crónicas, mientras que una longitud normal es compatible con proceso agudo pero no descarta enfermedad crónica. La ausencia de ectasia pielocalicial aleja la obstrucción urinaria.
g) la ERC de una nefropatía primaria de larga evolución puede adicionar trastornos neurológicos sensitivos y posibilidad de hallar osteodistrofia renal.
h) anemia, hipocalcemia e hiperfosfatemia son comunes y aparecen tanto en afectaciones renales agudas como crónicas.
EPIDEMIOLOGIA DE LA ERC6-9
Hay disparidades en la epidemiología de la insuficiencia renal terminal entre los países desarrollados que reflejan la diversidad étnica y racial, el envejecimiento poblacional y la prevalencia de diabetes y de hipertensión arterial. Además, es importante resaltar que en los países desarrollados la mayoría de los pacientes con IRC corresponden a la población ańosa.
FACTORES QUE INICIAN Y DETERMINAN PROGRESION A LA ERC6-8
Si bien la reducción de la función renal es de 0,75 a 1mL/min/ańo y se inicia entre los 40 y 50 ańos, la peoría de la función renal ocurre si existen otros factores de riesgo que juegan un rol tanto en el inicio como en la posterior progresión de la IRC:
FACTORES QUE POTENCIALMENTE PUEDEN CONTRIBUIR A LA PROGRESIÓN DE LA NEFROPATIA17
CAUSAS REVERSIBLES DE INSUFICIENCIA RENAL6-7
Si bien la mayoría de las nefropatías mencionadas tienen tendencia a la progresión de la insuficiencia renal, otras condiciones pueden revertir y mejorar la función deteriorada de los rińones.
HIPOPERFUSION RENAL Y DROGAS NEFROTOXICAS 6,8)
La hipovolemia en condiciones con vómitos, diarrea, uso de diuréticos, hemorragia, como también la hipotensión arterial que acompańa a insuficiencia cardíaca o al taponamiento pericárdico, también la sepsis o la administración de aminoglucósidos en dosis no ajustadas, AINEs, IECA, y la administración de iodados son todas situaciones que pueden evolucionar con recuperación parcial o total de la falla renal.
OBSTRUCCION DEL TRACTO URINARIO6-9
La obstrucción urinaria siempre debe ser considerada en un paciente con insuficiencia renal inexplicable. Las enfermedades de la próstata como causales de insuficiencia renal son menos comunes que las condiciones con hipoperfusión o tóxicas. Cuando se desarrolla una obstrucción lenta la diuresis se mantiene y no hay signos de enfermedad renal (ausencia de proteinuria y sedimento urinario blando). El diagnóstico generalmente surge con una ecografía renal, mostrando la dilatación de la vía excretora.
MANIFESTACIONES CLINICAS DE LA ERC8-24
La mayoría de los pacientes con ERC no tienen manifestaciones clínicas y la enfermedad renal se descubre fortuitamente como parte de una evaluación clínica general o por el estudio de una enfermedad no relacionada. Sin embargo, no es excepcional presentarse con signosintomatología del estadio terminal o urémico.
Dependiendo de la duración y severidad de la ERC los pacientes pueden manifestar debilidad, fatiga fácil, tendencia a vomitar esporádicamente, cambios en el estado mental con cierta obnubilación y eventualmente convulsiones. La hipertensión arterial es un hallazgo frecuente.
La anuria nunca es observada en la ERC o en la IRRP, y esta siempre indica IRA o obstrucción urinaria bilateral, necrosis cortical por complicaciones de un embarazo o un aneurisma disecante de aorta. La nicturia es expresión de la poliuria compensadora de la ERC y se inicia con FG entre 30 y 40 ml/min.
Las alteraciones clásicas de laboratorio incluyen el aumento de la creatinina y urea plasmáticas, acidosis y tendencia a la hipercalemia, anemia por déficit de eritropoyetina, aumento de la PTH (elevado remodelado óseo), que en algunos pacientes el nivel se incrementa solo por 2 o 3 veces, aunque también es posible con concentraciones reducidas de la hormona denotando alteraciones de bajo remodelado óseo, hiperfosfatemia e hipocalcemia. La orina contiene grados variables de proteinuria y el sedimento urinario puede mostrar persistencia de la actividad de la enfermedad de base o alteraciones poco significativas.
La gradual declinación de la función renal en los pacientes con ERC conduce a un estadio avanzado denominado enfermedad renal de estado final, que cursa con el clásico síndrome urémico.
MANIFESTACIONES CLÍNICAS DEL SINDROME UREMICO CRONICO8,9,23
Las imágenes de la ecografía renal muestran en la mayoría de los pacientes disminución de los tamańos. Es posible tamańos normales en diabéticos y con amiloidosis renal y en aquellos con insuficiencia renal de rápida progresión. Es probable encontrar numerosos quistes bilaterales sin agrandamiento del tamańo renal (multiquistosis) o en aquellos con múltiple quistes con historia familiar sugestivo de poliquistosis renal.
RECOMENDACIONES DIETETICAS EN LA ERC17,23
La desnutrición es común en los pacientes con ERC avanzada debido a inapetencia, disminución de la absorción intestinal y acidosis metabólica. Muchos estudios indican una fuerte correlación entre desnutrición y muerte.
La hipoalbuminemia es un índice de desnutrición que debe ser medido regularmente. Una dieta adecuada debe tener un aporte de 30 a 35 Kcal/Kg/d, 0.8 a 1.0g/kg/d de proteínas de alto valor biológico, sodio < 2000 mg/d, potasio 40 a 70 mEq/d, fósforo 600 a 800 mg/d, calcio 1400 a 1600 mg/d. Estas recomendaciones deben ajustarse a las necesidades individuales del paciente.
ANEMIA10-21
La anemia definida por una concentración de Hb < de 13g/dl en hombres y < de 12g/dl en mujeres, de tipo normocítica y normocrómica, se inicia en las categorías G3a a G5 y es causada por el déficit de formación renal de la eritropoyetina. Otros factores que contribuyen a la anemia son una menor disponibilidad de hierro, el relativamente frecuente estado de inflamación crónica que tienen los pacientes con ERC, déficit de folatos y vitamina B12, pérdidas ocultas digestivas, y enfermedades hematológicas primarias.
La prevalencia de la anemia es de 1% con GF de 60 mL/min, 9 % con FG de 30mL/min y de 33 a 67% con FG de 15mL/min. Como se ha establecido en las guias KDIGO 2012 el estudio de la anemia debe comenzarse con niveles de Hb < 12g/dL en mujeres y < de 13g/dL en hombres.
EVALUACIÓN Y DIAGNÓSTICO 23
La evaluación de la anemia debe definir su etiología, magnitud e impacto clínico, independientemente de la etapa evolutiva de la ERC. Inicialmente antes de comenzar el tratamiento debe realizarse la determinación de los siguientes parámetros:
El objetivo del tratamiento de la anemia en la ERC es alcanzar y mantener un nivel de Hb entre 10,5 y 12 g/dl, con ferritina > 100 ng/ml y TSAT > 20%.
TERAPÉUTICA23
El tratamiento se basa en el tratamiento con hierro y eritropoyetina humana, dependiendo del grado de ERC. La administración de hierro debe iniciarse cuando la Hb es < 11 g/dl con TSAT < 20% o ferritina < 100 µg/l. La dosis oral es de 100 a 200 mg/d de hierro elemental. Puede usarse la vía EV, que es de elección en los hemodializados con hierro sacarato 100mg/200mg diluido en 100 ml de solución fisiológica y lenta administración (30 a 60 min). Las dosis se adecuan a la respuesta y determinaciones de los parámetros de hierro.
Los agentes estimulantes de la eritropoyesis deben iniciarse si la Hb es inferior a 10 g/dl en dos determinaciones consecutivas, con eritropoyetina recombinante humana en dosis de 50 a 100 UI/kg semana en 3 aplicaciones subcutáneas. Las dosis subsiguientes se ajustan a la respuesta obtenida.
METABOLISMO MINERAL Y OSEO 19
Tanto la hiperfosfatemia, que comienza precozmente en las nefropatías debido a reducción de la carga filtrada de fosfato, como la deficiencia de la síntesis renal de 1,25 (OH2) D3 con la consecuente hipocalcemia, contribuyen al hiperparatiroidismo secundario y en algunos pacientes al desarrollo de enfermedad ósea renal, definida por alteraciones en la morfología ósea asociada a ERC, que solo puede diagnosticarse con biopsia ósea.
Inicialmente con FG > 30 ml/min estas alteraciones (aumento del fósforo y disminución de la calcemia) son compensadas con aumento de la síntesis de PTH. La restricción de fósforo de la dieta junto a los quelantes del fósforo limitan el desarrollo del hiperparatiroidismo secundario. La ingestión de calcio debe limitarse si hay evidencia de ateroesclerosis coronaria, arterial periférica, de tejidos blandos o calcifilaxis. Hay una fuerte asociación entre elevación del fósforo, calcio y PTH con ateroesclerosis.
HIPERPARATIROIDISMO SECUNDARIO 20
El hiperparatiroidismo secundario es debido a:
-
a) Retención de fosfato
b) Disminución del calcio libre ionizado
c) Disminución de 1,25-dihidroxivitamina D (calcitriol)
d) Aumento de la concentración del factor de crecimiento fibroblástico (FGF23) (péptido circulante que controla la concentración de fosfato sérico, secretado por osteocitos y osteoblastos en respuesta al calcitriol, aumento dietético del fosfato, PTH y calcio).
e) Expresión reducida del receptor de la vitamina D, del receptor sensor de calcio, del receptor del FGF23 y de klotho (es una proteína transmembrana producida por los osteocitos, que es requerida por el receptor del FGF23 para su activación) en la glándula paratiroidea
El tratamiento del hiperparatiroidismo secundario se establece con quelantes del fosfato, calcitriol o análogos de la vitamina D y calcimiméticos.
El tratamiento de la hiperfosfatemia incluye dieta con 800 a 1000 mg/d de fósforo. Si no se alcanzan los valores de fósforo séricos recomendados se agrega un quelante cálcico con una dosis total de calcio de hasta 2g/d, repartida con las comidas principales. Evitar la hipercalcemia.
Se recomienda un quelante no cálcico, como el carbonato de sevelamer en dosis de 800 a 1600 mg en cada comida principal, si existe hiperfosfatemia resistente al quelante cálcico, calcificaciones vasculares o tisulares, PTH menor de 150 pg/mL o calcifilaxis.
La PTH debe ser mantenida entre 150 y 300 pg/mL. Supresión de PTH por debajo de 150 pg/mL debe ser evitada porque ese nivel se asocia con enfermedad ósea adinámica.
Los niveles de fosforo adecuados se encuentran entre 3.5 y 5.5 mg/dL y las calcemias entre 8.4 y 9.5 mg/dL.
Déficit de 25(OH) D (calcidiol) < 30ng/mL debe indicarse tratamiento sustitutivo. La reposición del calcidiol depende de su concentración sérica. Así, con VD < 5ng/mL 50000 UI una vez por semana por 12 semanas y 50000UI por mes. Con VD entre > 5 y < 15 ng/mL 50000 UI una vez por semana por 4 semanas y 50000 UI por mes y con VD > 16 y < 30 ng/mL 50000 UI por mes.
El calcitriol (1,25(OH)2D) es la forma activa de la VD producida en el rińón, y primera opción de tratamiento para el hiperparatiroidismo secundario, después de normalizar la fosfatemia, hipocalcemia y haber suplementado con calcidiol. Una dosis inicial recomendada es de 0.5 mcg/sesión de diálisis (trisemanal). En diálisis peritoneal la dosis es similar. No se debe exceder los 7 u 8 mcg/semana.
Cinacalcet es un calcimimético que se indica para reducir los niveles de PTH > 300 pg/mL con concentraciones de calcio sérico > 8.4mg/dL, aún con hiperfosfatemia. La dosis inicial es de 30 mg/d, que puede aumentarse a 60 mg/d.
Las alteraciones estructurales óseas más frecuentes en la IRC son la osteitis fibrosa quística (caracterizada por un elevado turnover óseo debido a hiperparatiroidismo secundario), osteomalacia (bajo turnover óseo con mineralización alterada), enfermedad ósea adinámica (presenta bajo turnover óseo por supresión excesiva de la paratiroides) y la osteodistrofia urémica mixta (combina alto o bajo turnover con mineralización anormal). Existe una quinta osteopatía urémica que es la amiloidosis relacionada a la diálisis en pacientes en diálisis después de varios ańos con quistes óseos (que resulta de los depósitos de amiloide secundarios a la beta2 microglobulina elevada).
HIPERPARATIROIDISMO TERCIARIO 20
Algunos pacientes con ERC desarrollan una marcada elevación de la PTH asociada a hipercalcemia que no se explica por la administración de carbonato de calcio ni de calcitriol. Suelen requerir paratiroidectomía.
ACIDOSIS METABOLICA11-12
La mayoría de los individuos producen aproximadamente 15,000 mmol de dióxido de carbono y entre 50 y 100 meq de ácidos no volátiles diariamente.
El balance ácido-base se regula mediante la eliminación de dióxido de carbono por los pulmones manteniendo normal la presión parcial de dióxido de carbono (PCO2) y con la excreción normal de los ácidos no volátiles por los rińones (1 meq/Kg/día) mediante la eliminación urinaria de los iones hidrógeno como acidez titulable y amonio. La concentración del ion hidrógeno está determinada por la relación de la PCO2 y la concentración de bicarbonato plasmático.
DESARROLLO DE LA ACIDOSIS METABOLICA 11, 12
Esta puede desarrollarse como resultado de una de las siguientes alteraciones:
-
a) disminución de la excreción renal de ácidos
b) aumento de la producción de ácidos no volátiles
c) pérdida de bicarbonato
En la IRC con FG debajo de 40 a 50ml/min la excreción de amonio se reduce y en consecuencia se retienen iones hidrógeno. Además disminuye la excreción de ácido titulable (ácido fosfórico) que también contribuye a la acidosis metabólica. La retención ácida es amortiguada por el bicarbonato del líquido extracelular, buffers tisulares y óseos. El bicarbonato sérico desciende a < 22meq/L y es muy raro que descienda a 10 mEq/L. Bicarbonato sérico menor a 22 mEq/L es el nivel para iniciar tratamiento con bicarbonato de sodio 0.5 a 1 mEq/kg/d para llevar la concentración de bicarbonato entre 23 y 29 mEq/L. La suplementación crónica o prolongada con bicarbonato requiere de un cuidadoso monitoreo de la volemia y líquido extracelular por el aporte de sodio.
CONSECUENCIAS DE LA ACIDOSIS METABOLICA EN LA IRC 11, 12
AUMENTO DE LA MORTALIDAD RELACIONADA A LA ACIDOSIS11, 12
La mayoría de los estudios observacionales en pacientes con ERC en estadios G4 y G5 muestran un significativo aumento de la mortalidad asociada a la acidosis metabólica.
RIESGO CARDIOVASCULAR 16,22
La ERC y la proteinuria aumentan el riesgo de enfermedad cardiovascular (ECV) a través de enfermedad coronaria, cerebrovascular y arterial periférica y es más probable que estos pacientes mueran por estas complicaciones que por la progresión de la insuficiencia renal. Otros factores adicionales de riesgo para ECV son
FACTORES DE RIESGO PARA DESARROLLAR ENFERMEDAD CARDIOVASCULAR 16,22
USO DE CONTRASTES RADIOLOGICOS 24
En pacientes con FG < 60 ml/min/1,73 m2 que vayan a recibir un contraste yodado, se recomienda:
Con respecto a la utilización de contrastes basados en gadolinio, se recomienda evitar su uso en pacientes con FG estimado < 30 ml/min/1,73 m2 (GR 1B).
Asimismo, se recomienda no utilizar preparados orales con fosfatos para la preparación intestinal en pacientes con FG estimado< 60 ml/min/1,73 m2 .
INFECCIONES14,17,23
Las infecciones son la segunda causa de muerte después de la ECV en pacientes con ERC. Estas se deben tanto a defectos de la inmunidad celular como humoral, que determinan un estado de inmunosupresión crónica. El riesgo de infección bacteriana, particularmente pulmonar o urinaria aumenta con la declinación de la función renal. Es recomendable indicar vacunación para el virus de la influenza y neumococo.
DISLIPIDEMIA22
Es común encontrar dislipemia en la ERC. La alteración frecuente es la hipertrigliceridemia con colesterolemia normal.
Datos limitados sugieren que la disminución de la hiperlipemia con estatinas podría enlentecer la progresión de la ERC.
HIPERTENSION ARTERIAL16,22
La hipertensión arterial se encuentra entre el 80 a 90% de los pacientes con ERC. El tratamiento de la misma es conveniente para enlentecer la progresión de la nefropatía y reducir el riesgo de complicaciones cardiovasculares. La expansión de volumen que presentan invariablemente la mayoría de estos pacientes, aún en ausencia de edema, contribuye a la elevación de la presión sanguínea.
Por ello es más recomedable iniciar tratamiento con diuréticos del asa como la furosemida y de ser necesario agregar IECA o BRA. El nivel de presión sanguínea recomendable debe ser individualizado considerando la edad del paciente, comorbilidades, ECV subyacente, riesgo de progresión de la nefropatía y tolerancia al tratamiento indicado.
La presión sanguínea óptima en un hipertenso con ERC no resulta clara, pero conociendo que la FG disminuye con presión arterial media mayor de 100mmHg, parece razonable proponer diastólicas entre 80 y 85 mmHg, con presión sistólica por debajo de 140 mmHg.
SOBRECARGA DE VOLUMEN 14,22
El balance del sodio y del volumen intravascular son mantenidos frecuentemente por mecanismos homeostáticos hasta que el FG se encuentra entre 10 y 15 ml/min. Sin embargo el paciente con ERC es menos respondedor a una rápida ingesta de sodio y tiene facilidad para la sobrecarga de líquido. Esta puede manejarse con reducción de la ingesta de sodio a < de 2g/d y de ser necesario con diuréticos del asa.
HIPERCALEMIA 18
La capacidad de mantener la excreción de potasio en niveles normales en ERC es posible con secreción de aldosterona y flujo tubular distal normales. Así, la hipercalemia puede desarrollarse en pacientes oligúricos, en aquellos con dieta rica en potasio, en hipercatabólicos o con hipoaldosteronismo, debido a veces a la administración de IECA y BRA. Algunas medidas que ayudan a mejorar la hipercalemia son una dieta pobre en potasio, entre 40 y 70 mEq/d, evitar los AINEs y reducir IECA O BRA. Eventualmente se puede recurrir a resinas de intercambio catiónico.
DISFUNCION SEXUAL 14,17,22
En los pacientes con ERC avanzada se observan frecuentemente anormalidades sexuales y de la función reproductiva. El 50% de los hombres en diálisis presentan disfunción eréctil, disminución de la líbido y declinación de la frecuencia del intercurso sexual. Las mujeres notan alteraciones menstruales hasta amenorrea y el embarazo es raro con creatinina superior a 3 mg/dL.
TRATAMIENTO FARMACOLÓGICO DE LA DISLIPEMIA EN ADULTOS: CUÁNDO?24

DERIVACION AL NEFROLOGO23
Los pacientes con ERC deben ser derivados a un nefrólogo cuando el FGe o el medido se encuentra en <30mL/min, esencialmente para discutir y planear el tratamiento sustitutivo de la función renal a seguir. Hay evidencia que la derivación precoz y manejo por un nefrólogo se asocia a un menor gasto médico, morbilidad y mortalidad.
La derivación a nefrología en cualquier estadio debe realizarse en las siguientes circunstancias:
REFERENCIAS
-
1. National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39:S1
2. Levey AS, Coresh J, Balk E, et al. National Kidney Foundation practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Ann Intern Med 2003; 139:137.
3. Levey AS, Eckardt KU, Tsukamoto Y, et al. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2005; 67:2089.
4. Wanner C, Tonelli M and the Kidney Disease: Improving Global Outcomes Lipid. Guideline Development Work Group Members. KDIGO Clinical Practice Guideline for Lipid Management in CKD: summary of recommendation statements and clinical approach to the patient. Kidney International (2014) 85, 1303-1309
5. Recomendaciones de Práctica Clínica de la SLANH para el tratamiento de la anemia en el paciente con Enfermedad Renal Crónica. Nefrología Latinoamericana. National Kidney Foundation. Clinical Practice Guidelines and Clinical Practice Recommendations for Anemia in Chronic Kidney Disease. Am J. Kidney Dis 2006; 47 (Suppl 3): 11-145.
6. KDOQI Clinical Practice Guideline and Clinical Practice Recommendations for Anemia in Chronic Kidney Disease; 2007 Update of Hemoglobin Target. Am J Kidney Dis 2007; 50: 471-530.
7. Moist LM, Foley RM, Barret BJ, Madore F, White CT, Klarenbach SW, Culleton BF, Tonelli M, Manns BJ. Clinical Practice Guidelines for evidence-based use of erythropoietic-stimulating agents. Kidney Int 2008; 74 (Suppl 110): S12-S18.
8. Bradbury BD, Fissell RB, Albert JM, et al. Predictors of early mortality among incident US hemodialysis patients in the Dialysis Outcomes and Practice Patterns Study (DOPPS). Clin J Am Soc Nephrol 2007;2:89.
9. Stack AG. Impact of timing of nephrology referral and pre-ESRD care on mortality risk among new ESRD patients in the United States. Am J Kidney Dis 2003;41:310.
10. Astor BC, Muntner P, Levin A, et al. Association of kidney function with anemia: the Third National Health and Nutrition Examination Survey (1988-1994). Arch Intern Med 2002;162:1401.
11. Bailey JL. Metabolic acidosis: an unrecognized cause of morbidity in the patient with chronic kidney disease. Kidney Int. Suppl 2005;S15.
12 .Garibotto G, Sofia A, Robaudo C et al. Kidney protein dynamics and ammoniagenesis in humans with chronic metabolic acidosis. J Am Soc Nephrol 2004;15:1606.
13. Krant JA, Kurtz I. Metabolic acidosis of CKD: diagnosis, clinical characteristics, and treatment. Am J Kidney Dis 2005;45:978.
14. Yu HT. Progression of chronic renal failure. Arch Intern Med 2003;163:1417.
15. Hebert LA, Greene T, Levey A, et al. High urine volume and low urine osmolality are risk factors for faster progression of renal disease. Am J Kidney Dis 2003;41:962.
16. Ejerblad E, Fored CM, Lindblad P, et al. Association between smoking and chronic renal failure in a nation wide population-based case-control study. J Am Soc Nephrol 2004;15:2178.
17. Brantsma AH, Atthobari J, Bakher SJ, et al.What predicts progression and regression of urinary albumin excretion in the nondiabetic population? J Am Soc Nephrol 2007;18:637.
18. Delmez JA, Slatopolsky E. Hyperphosphatemia: its consequences and treatment in patients with chronic renal disease. Am J Kiney Dis 1992; 19:303.
19. Hruska KA, Teitelbaum SL. Renal osteodystrophy. N Engl J Med 1995; 333:166.
20. Muntner P, Jones TM, Hyre AD, et al. Association of serum intact parathyroid hormone with lower estimated glomerular filtration rate. Clin J Am SOC Nephrol 2009;4:186.
21. Hsu CY, McCulloch CE, Curhan GC. Epidemiology of anemia associated with chronic renal insufficiency among adults in the United States: results from the Third National Health and Nutrition Examination Survey. J Am Soc Nephrol 2002; 13:504.
22. Appel G. Lipid abnormalities in renal disease. Kidney Int 1991; 39:169.
23. KDIGO Clinical Practice Guideline for lipid Management in Chronic Kidney Disease. Kidney Int Suppl 2013;3:263.
24. http://www.fda.gov/cder/drug/infoSheets/HCP/gcca_200705.htm (Accessed on October 10, 2008).
CORRESPONDENCIA:
Dra. Gabriela A. Gonzalez
División Nefrología
Hospital de Clínicas Jose de San Martín.
Universidad de Bueno Aires.
Buenos Aires. Argentina
Email: gagonzalez @ intramed.net
Comentario de la revisora Dra. Mariana Ciocchini. Instituto Daomi - Buenos Aires, Argentina
Si bien, en las personas jóvenes, la disminución de la tasa de filtración glomerular (TFG) permite "per se" el diagnóstico de la enfermedad renal crónica (ERC) desde el estadio II en adelante, no ocurre lo mismo con los adultos mayores. En éstos, hay que tener presente la caída de la TFG que ocurre con el envejecimiento y comparar la TFG del paciente con la esperada para su edad calculada con la fórmula de Keller. Asimismo, para no sobrediagnosticar la ERC deben considerarse las alteraciones fisiopatológicas que la acompańan pero que no se hallan en la senescencia renal1.
Otra consecuencia de la senescencia renal es que la insuficiencia renal aguda prerrenal, en los ancianos, se presenta como un síndrome intermedio en el cual los parámetros de laboratorio habituales pierden su utilidad diagnóstica2.
Referencias
1) Musso CG, Jauregui JR. How to differentiate renal senescence from chronic kidney disease in clinical practice. Postgrad Med 2016;128:716-21.
2) Musso CG, Luque K, reynaldi J et al. Síndrome Intermedio: Un patrón típico de Insuficiencia Renal Aguda en el Anciano. Electron J Biomed 2004;3:36-38.
Comentario de la revisora Susana Gabriela Pérez MD. Especialista en Nefrología. Posgrado de Efectividad Clínica, Analista de Datos Médicos en Diaverum. Argentina.
La diabetes, la hipertensión y el envejecimiento son los principales factores de riesgo para desarrollar la enfermedad renal crónica. Según un estudio publicado por Organización Panamericana para la Salud (OPS) / Organización Mundial de la Salud (OMS)en el ańo 2015, un 10% de la población mundial tiene enfermedad renal crónica y uno de cada diez adultos en el mundo desarrollará enfermedad renal crónica.
En el trabajo se presenta una revisión muy completa y clara sobre el tema de la enfermedad renal crónica. Como es sabido, algunos pacientes se recuperan pero otros continúan hasta el estadio final de su evolución, cuyo tratamiento es la terapia de reemplazo renal: hemodiálisis, diálisis peritoneal o trasplante renal.
La OPS y Sociedad Latinoamericana de Nefrología e Hipertensión están impulsando acciones para elevar la tasa de tratamiento de sustitución de la función renal hasta 700 pacientes por millón de habitantes en cada país de Latinoamérica para 2019.
