Indice del volumen Volume index
Comitť Editorial Editorial Board
Comitť CientŪfico Scientific Committee
- Derrame pleural
- Derrame pericŠrdico
- Ascitis
- LŪquido articular
- Humor vŪtreo
- LCR
PLANES DE HIDRATACI”N PARENTERAL.
Segunda parte: el modelo compartimental.
Lucas FernŠndez Otero
ClŪnica Mťdica Hospital Italiano de San Justo. Universidad Nacional de La Matanza. Instituto Universitario del Hospital Italiano.
Buenos Aires. Argentina.
Email: lucas.fernandez @ hospitalitaliano.org.ar
Rev Electron Biomed / Electron J Biomed 2020;1:20-26.
Comentario del revisor Dr. Carlos G. Musso, MD. PhD. Facultad de Ciencias de la Salud. Universidad Simůn Bolivar Barranquilla, Colombia.
Comentario del revisor Dr. Manuel Vilas, MD. Nefrůlogo miembro del Comitť de NefrologŪa CrŪtica de la Sociedad Argentina de Terapia Intensiva.
RESUMEN
La hidrataciůn parenteral endovenosa es una prŠctica cotidiana en la medicina moderna. Cobrů fuerte impulso luego de la segunda guerra mundial, siendo hoy un pilar fundamental en el manejo del paciente internado.
En esta segunda parte del presente trabajo se describen los fundamentos para su uso, sus indicaciones, las soluciones de uso mŠs habitual, su distribuciůn en los distintos compartimentos corporales, su interacciůn en los mismos compartimentos en distintas situaciones clŪnicas habituales como deshidrataciůn, sobrecarga de volumen, cirrosis y sepsis.
PALABRAS CLAVE: Hidrataciůn, parenteral, terapia, fluidos.
ABSTRACT:
Intravenous therapy is a daily practice in modern medicine. It gained strong momentum after the Second World War, being today a fundamental pillar in the management of hospitalized patients.
In this second part of the present work describes the rationale for its use, its indications, the most commonly used solutions, its distribution in the different body compartments, its interaction in the same compartments in different common clinical situations such as dehydration, volume overload, cirrhosis and sepsis.
KEY WORDS: Therapy, fluids, hydration, parenteral
La PRIMERA PARTE, fue expuesta anteriormente
SEGUNDA PARTE: El modelo compartimental:
Para entender la distribuciůn de las distintas soluciones que se pueden utilizar a la hora de confeccionar un PHP es menester entender la distribuciůn de los lŪquidos corporales en distintos compartimentos. La cantidad de agua corporal que se encuentra en un organismo dependerŠ de la edad y el sexo del paciente, asŪ como tambien de la relaciůn entre masa magra y grasa que tiene un individuo1. De forma general se puede decir que la cantidad de agua corporal total tendrŠ la siguiente relaciůn con el peso en kilogramos:
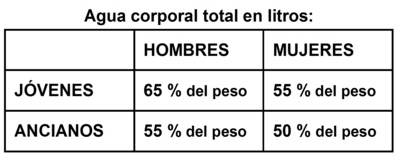
Los niŮos pequeŮos pueden tener 75 - 80% del peso en agua, en tanto un obeso de 150 kg puede tener tan solo 30%.
Vamos a representar al cuerpo humano en compartimentos teůricos y esquemŠticos a los efectos de comprender la distribuciůn de los lŪquidos, el comportamiento de las soluciones de infusiůn y distintos procesos patolůgicos que alteran la distribuciůn y composiciůn de estos compartimentos.
De manera esquemŠtica los lŪquidos se distribuyen en dos grandes compartimentos: el LŪquido Intracelular (LIC) y el lŪquido extracelular (LEC). La relaciůn entre ambos es de 2/3 para el LIC y ¼ para el LEC.
A su vez el LEC se divide en dos compartimentos: el intersticio que representa ĺ del LEC y el intravascular que representa ¼ del LEC2.
Asi en un varůn de 30 aŮos de 70 kg con BMI normal la distribuciůn de lŪquidos serŪa:
Agua Corporal total: 70 x 0.65: 45 litros
LIC: 45 x 2/3: 30 litros
LEC: 45 x 2/3: 15 litros
intersticio: 15 x ¾: 11 litros
intra vascular: 15 x ¼: 3.75 litros
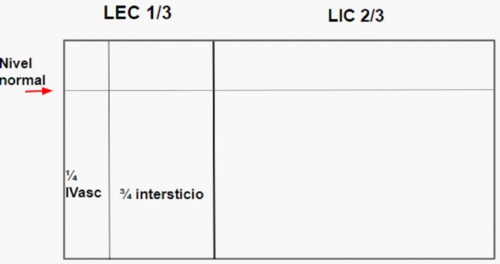
Los distintos compartimentos pueden ser evaluados en la prŠctica clŪnica lo que ayuda enormemente a hacer un diagnůstico de situaciůn y planificar los planes de hidrataciůn.
Evaluaciůn del Intravascular:
Es tal vez el mŠs sencillo de todos. Se realiza a travťs del examen fŪsico distintos tipos de mťtodos complementarios:
1) Frecuencia cardŪaca y Tensiůn arterial supina y erecta, buscando ortostatismo como signo de contracciůn intravascular
2) Ingurgitaciůn de venas yugulares.
3) Presiůn venosa central. PVC
4) Presiůn de enclavamiento pulmonar (wedge).
5) EcografŪa de vena cava inferior3.
(distensiůn y comportamiento respiratorio)
6) Evaluaciůn hemodinŠmica : variaciůn de la onda de pulso y descarga sistůlica latido a latido. (Si la variabilidad es mayor al 13% hay hipovolemia). Requiere monitoreo arterial.
7) Maniobras dinŠmicas: elevaciůn de mmii con posiciůn supina (genera una auto transfusiůn de 300 cc desde los mmi hacia la circulaciůn central) con esto aumenta la descarga sistůlica, aumenta el gasto cardiaco y baja la variabilidad del volumen sistůlico (requiere monitoreo invasivo arterial)4.
8) Laboratorio: urea creatinina y Šcido ķrico. Fena, Feu, y alcalosis metabůlica. Son ķtiles marcadores de contracciůn.
9) Na urinario: es el marcador mŠs ķtil para evaluar la volemia arterial efectiva. (Ver mŠs adelante)2.
Evaluaciůn del intersticio:
1) Edema: se localiza en mmii por ambas caras anterior y posterior, flancos, zona sacra. Es importante entender que puede existir una fase intermedia en el cual el intersticio ha aumentado en volumen pero aķn NO hay edemas. (LEC alto sin edemas). En algunos pacientes se necesita entre 5 y 6 litros de exceso del compartimiento para que sean clŪnicamente evidentes los edemas. En la mayorŪa de las personas se requiere un mŪnimo de 3 litros. El proceso můrbido tŪpico que cursa con LEC alto sin edemas es el SSIHAD que errůneamente se lo clasifica con LEC normal.
2) Intersticio pulmonar: desarrollada en los ķltimos aŮos la tťcnica es por ecografŪa, siendo altamente sensible5.
Existe ademŠs una serie de compartimentos que pertenecen a LEC que se conocen como lŪquidos transcelulares, ellos son:
El lŪquido dentro del tubo digestivo ya sea en condiciones normales o en Ūleo se lo considera por fuera del organismo y constituye el llamado 3er espacio, formalmente NO pertenece a ninguno de los compartimentos anteriores.
Evaluaciůn del compartimiento Intracelular (LIC)
En la prŠctica es difŪcil de cuantificar. Se lo puede hacer a travťs de dos medidas:
1) Bioimpedanciometria elťctrica en la cual se determina el volumen de LEC y el LIC.
2) Indirectamente a travťs de la osmolaridad plasmŠtica ya que en la enorme mayorŪa de los casos hay una correlaciůn inversa entre el volumen del LIC y la osm p.2.
Distribuciůn de las distintas soluciones en los distintos compartimentos corporales:
Analizaremos a continuaciůn cůmo se distribuyen las distintas soluciones de uso habitual en los distintos compartimentos. Imagine el lector que el organismo es una gran pecera, a la que solo se tiene acceso por el compartimento IV, de hecho la absorciůn de lŪquidos y nutrientes pasa rŠpidamente al intravascular, asŪ como tambiťn por definiciůn las infusiones endovenosas.
La hidrataciůn en el tejido celular subcutŠneo fue anterior a la utilizaciůn de las vŪas endovenosas. Estas ķltimas cobran mayor importancia luego de la segunda guerra mundial. En la actualidad la vŪa subcutŠnea se utiliza en cuidados paliativos con el objetivo de proporcionar confort a un paciente con agotamiento de accesos vasculares. De ahora en adelante asumimos toda administraciůn en el compartimento intravascular6.
1. Dextrosa 5%
Si infundimos un litro de Dx5%, dado que es una soluciůn libre de sodio se distribuye rŠpidamente en todos los compartimentos corporales. De 1 litro solo quedarŠ en el intra vascular 83 ml. Por lo tanto NO debe expandirse el intra vascular con dextrosa. En la prŠctica se reserva el tťrmino expandir al aumento de volumen del intra vascular o del LEC en su conjunto.

Como se ve la dx5% es el equivalente a hidratar con agua. Se distribuye segķn los volķmenes de los distintos compartimentos segķn la regla del 2/3 y 1/3 para LEC y LIC y a su vez ¾ y ¼ para el LEC. Es una verdadera hidrataciůn muy ķtil en quien ha perdido agua libre o pura. No es una expansiůn, sino una verdadera hidrataciůn de todos los compartimentos. AdemŠs la dextrosa es rŠpidamente ingresada a las cťlulas y metabolizada en situaciones de secreciůn de insulina normal, por lo que no contribuye a mantener la osmolaridad en forma persistente, la misma depende fundamentalmente de las sales de sodio en el LEC y de las de potasio en el LIC.
Dado que la infusiůn de dx 5% diluye uniformemente estas sales, se observa en la figura que la osmolaridad baja de 280 a 275 mosm kg uniformemente (el valor absoluto de cuanto desciende se puede calcular con exactitud pero tan solo se expresa un valor tentativo, para entender que la osmolaridad baja tras la administraciůn de esta infusiůn). Esta circunstancia en condiciones fisiolůgicas normales producirŪa una supresiůn de la secreciůn de ADH neurohipofisiaria con lo cual se producirŪa una diuresis acuosa que eliminarŪa el exceso de agua volviendo la osmolaridad a su valor normal7.
2. Soluciůn Fisiolůgica, Ringer lactato y Dextrosa 5% en clna 0.9%.
Son los tŪpicos cristaloides, defienden el volumen del LEC por lo que distribuyen por completo en el mismo con la relaciůn ¼ y ¾. Como se verŠ en la figura no producen ninguna modificaciůn de la osmolaridad ya que son isotůnicos. No pasan al espacio intracelular. Son ideales para la expansiůn intravascular ya que una parte sustancial queda retenida en dicho compartimento.
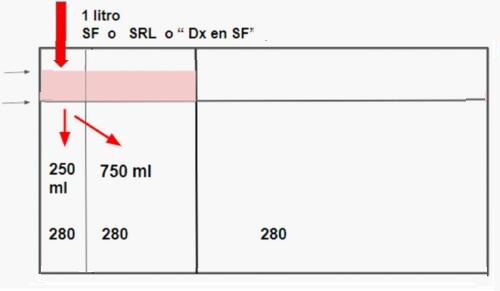
En condiciones normales, luego de esta expansiůn del LEC se producen mecanismos natriurťticos fisiolůgicos (aumenta el pťptido natriurťtico atrial y se suprime la aldosterona ), que producen eliminaciůn del sodio administrado en exceso. Estos mecanismos pueden ser deficitarios y/ o lentos en pacientes con cardiopatŪa, pudiendo generar sobrecarga de volumen. Los pacientes con insuficiencia cardŪaca avanzada tienen bajo el gasto cardŪaco y por lo tanto bajo el volumen arterial efectivo. Esto genera que los mecanismos de regulaciůn del volumen se disparen a pesar de la sobrecarga hacia la inhibiciůn de la natriuresis, inhibiciůn del pťptido atrial natriurťtico y aumento de la aldosterona.
3. Soluciůn Fisiolůgica 0.45%. "Medio salino"
Una forma esquemŠtica de entender su distribuciůn es descomponerla en dos mitades. Un litro de medio salino equivale a medio litro de agua + medio litro de clna 0.9% (sf).
AsŪ tendremos las siguiente distribuciůn:
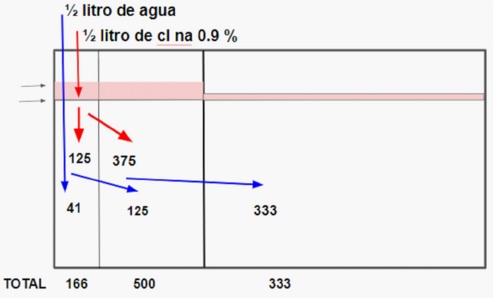
Como se ve es una situaciůn intermedia entre las otras dos produciendo mŠs expansiůn del LEC que el dextrosado pero menos que el fisiolůgico. Produce una leve disminuciůn de la osmolaridad en todos los compartimentos aunque menor que la dextrosa.
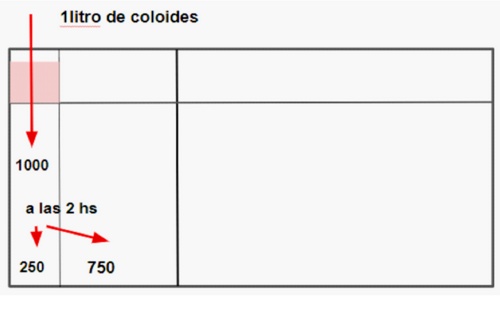
4. Coloides:
Tienen la propiedad de quedar retenidos en el compartimiento intravascular ejerciendo fuerte presiůn coloidosmůtica. La mayorŪa de las formulaciones tienen igual cantidad de sodio que la soluciůn fisiolůgica. Como comentamos en el capŪtulo anterior la vida media es de 1 a 2 horas metabolizandose rŠpidamente. Pasado este tiempo se comportan como un cristaloide distribuyendose en todo el LEC.
Tienen la capacidad teůrica de una expansiůn mŠs eficiente 8, pero como hemos comentado su elevado costo, las reacciones adversas (alergia, alteraciones de la coagulaciůn, priones etc) y la falta de resultados con puntos finales clŪnicos de importancia (mortalidad, estancia hospitalaria, inicio de ARM), ha hecho que el debate de su administraciůn continķe en la actualidad luego de 20 aŮos de investigaciůn.
REFERENCIAS
1.- Ramirez de PeŮa D, Almanza D, Ńngel LA, Others. Estimaciůn del agua corporal total y del peso seco usando impedancia bioelťctrica tetrapolar de multifrecuencia en pacientes en hemodiŠlisis. Universidad Nacional de Colombia, Unidad Renal Fundaciůn Hospital San Carlos, Cruz Roja y Centro de Investigaciůn. Revista de la Facultad de Medicina. 2015;63:19-31.
2.- Rose BD. Transtornos de los electrolitos y del equilibrio Šcido-base. 2001; Available from: http://www.sidalc.net/cgi-bin/wxis.exe/?IsisScript=AGRIUAN.xis&method=post&formato=2&cantidad=1&expresion=mfn=021389
3.- Citilcioglu S, Sebe A, Ay MO, Icme F, Avci A, Gulen M, et al. The relationship between inferior vena cava diameter measured by bedside ultrasonography and central venous pressure value. Pak J Med Sci Q. 2014;30:310-315.
4.- Limachi Choque AM. Evaluacion del deficit de volumen con la determinacion del diametro de vena cava inferior por ecografia y la maniobra de elevacion pasiva de miembros inferiores. Residencia Medica-Medicina CrŪtica y Terapia Intensiva; RM. MC yTI.-002/16; 2016. Available from: http://ddigital.umss.edu.bo:8080/jspui/handle/123456789/5202
5.- Macho JT, de Casasola SŠnchez GG. EcografŪa pulmonar, paradigma de la ecografŪa clŪnica [Internet]. Rev ClŪn Esp. 2020. Available from: http://dx.doi.org/10.1016/j.rce.2020.03.006
6.- FŁrst P, LundstrŲm S, Klepstad P, Strang P. Continuous subcutaneous infusion for pain control in dying patients: experiences from a tertiary palliative care center. BMC Palliat Care. 2020;19:172.
7.- Maxwell MH, Kleeman CR (ed). Clinical Disorders of Fluid and Electrolyte Metabolism. McGraw Hill, New York, 1962.
8.- Martin GS, Bassett P. Crystalloids vs. colloids for fluid resuscitation in the Intensive Care Unit: A systematic review and meta-analysis. J Crit Care. 2019;50:144-154.
CORRESPONDENCIA:
Lucas FernŠndez Otero
ClŪnica Mťdica Hospital Italiano de San Justo.
Universidad Nacional de La Matanza.
Buenos Aires. Argentina.
Email: lucas.fernandez @ hospitalitaliano.org.ar
